8 Minuten
Mikroplastik wurde in menschlichen Knochen nachgewiesen
Mikroplastik und noch kleinere Nanoplastikpartikel – oft aus fossilen Rohstoffen hergestellt und typischerweise kleiner als 5 mm – werden zunehmend im menschlichen Körper nachgewiesen. Eine neue Synthese von 62 Studien zeigt, dass diese Partikel bis tief in das Skelettgewebe vordringen können, einschließlich des Knochenmarks, und möglicherweise Stoffwechselvorgänge und Knochenwachstum stören. Die Übersichtsarbeit fasst Befunde aus Analysen menschlichen Gewebes, Tierexperimenten und Zellkulturstudien zusammen, um potenzielle Risiken für die Knochengesundheit darzulegen.
Hinweise und Eintrittspfade ins Knochengewebe
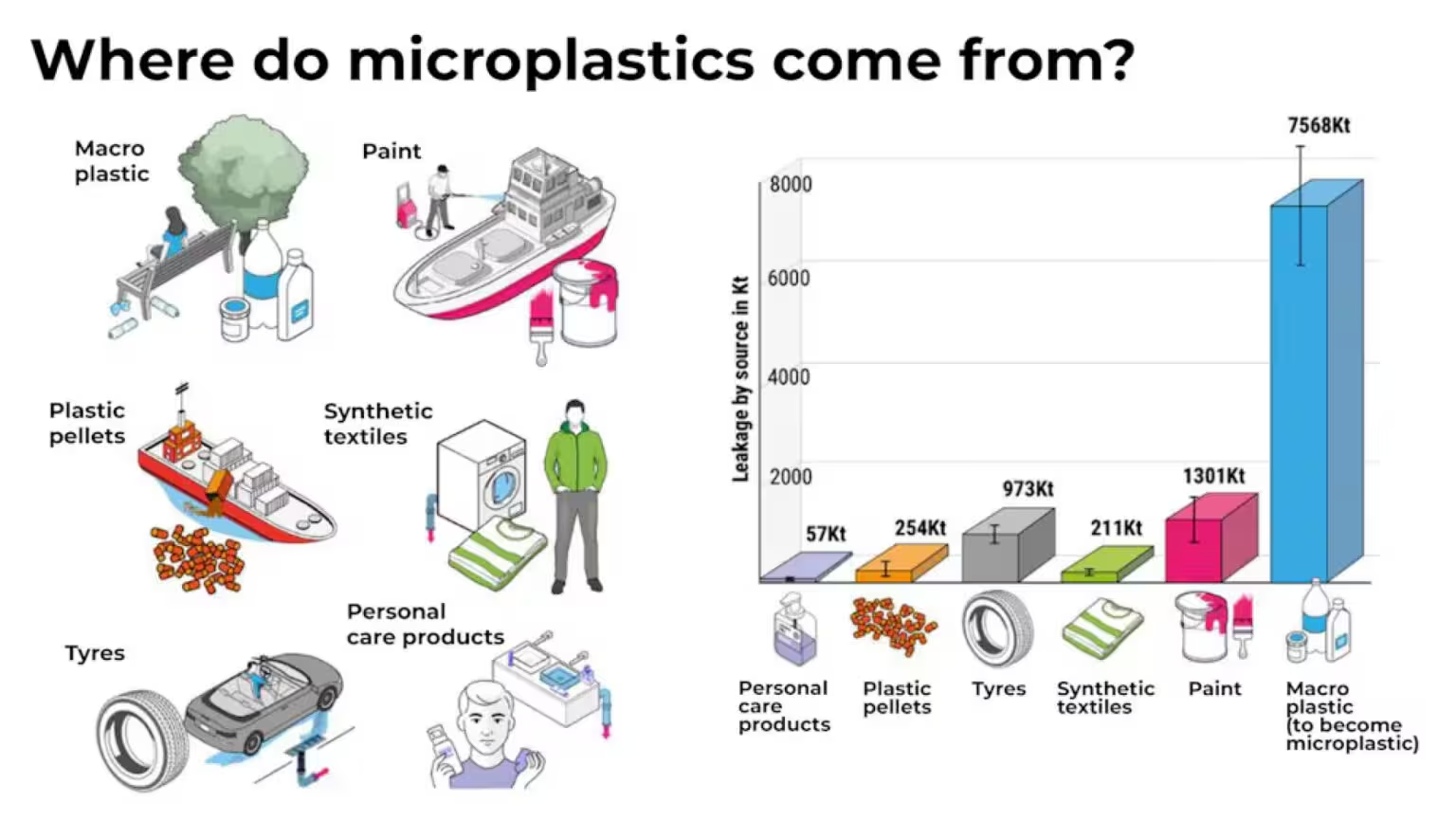
Quellen von Mikroplastik
Mehrere in der Übersichtsarbeit berücksichtigte Humanstudien berichten von Mikroplastikpartikeln in Knochenproben. Der plausibelste Eintrittsweg ist die Aufnahme über den Darm mit anschließender Translokation in den Blutkreislauf nach Ingestion, gefolgt von Verteilung zu inneren Organen und Geweben. Tiermodelle bestätigen diesen Weg weitgehend: Aufgenommene Partikel wandern in innere Gewebe und Laboranalysen zeigen Akkumulationen in Knochen und Knochenmark. Zusätzlich zu oraler Aufnahme können inhaliertes Mikroplastik und transdermale Exposition belastende Beiträge leisten, auch wenn die Quantifizierung dieser Wege für Skelettgewebe noch unzureichend ist.
Auf zellulärer Ebene zeigen Versuche mit knochenabgeleiteten Zelllinien wiederkehrende biologische Effekte. Die Exposition gegenüber Mikroplastik kann die Zellvitalität vermindern, vorzeitige zelluläre Seneszenz (Alterserscheinungen der Zelle) beschleunigen, die Differenzierung von Stammzellen zu osteogenen (knochenbildenden) Zellen verändern und entzündliche Signalwege aktivieren. Solche lokalen zellulären Veränderungen gelten als wahrscheinlicher Mechanismus für die eingeschränkte Knochenbildung, die in einigen Tierstudien beobachtet wurde. Diese Effekte wurden in unterschiedlichen Modelltypen gefunden, von kurzen akuten Expositionen bis hin zu längeren, wiederholten Expositionen, was auf mehrere mögliche biologisch relevante Wirkungspfade hinweist.
Auswirkungen auf Knochenwachstum und -festigkeit
Tierexperimente in der untersuchten Literatur dokumentieren verringertes Skelettwachstum nach Exposition gegenüber Mikro- und Nanoplastik. Die Partikel scheinen das Gleichgewicht zwischen Osteoblasten (knochenbildenden Zellen) und Osteoklasten (knochenabbauenden Zellen) zu stören. Wenn Osteoklasten in ihrer Funktion verändert werden, kann die Knochenumbau- und Reparaturfähigkeit beeinträchtigt werden, was zu schwächerer Knochenarchitektur, vermehrten Deformationen und einem höheren Frakturrisiko in experimentellen Tiermodellen führt. Besonders Besorgnis erregend sind Befunde in Modellen sich entwickelnder oder junger Tiere, bei denen gestörte Wachstumsprozesse langfristige strukturelle Nachteile nach sich ziehen können.
Mechanistisch werden mehrere Pfade diskutiert: physische Belastung durch die Partikel in Gewebe, toxikologische Effekte durch an der Oberfläche gebundene Schadstoffe (wie persistente organische Schadstoffe oder Metalle) und indirekte Effekte über Entzündungsreaktionen und oxidativen Stress. Diese Mechanismen können einzeln oder kombiniert die Differenzierung von mesenchymalen Stammzellen zugunsten eines nicht-osteogenen Schicksals verändern, die Produktion von knochenmatrixbildenden Proteinen hemmen und die Balance von Auf- und Abbauprozessen stören. Langfristig kann dies die mechanische Integrität des Knochens reduzieren und die Anfälligkeit für alters- oder traumaspezifische Brüche erhöhen.
Der Medizinforscher Rodrigo Bueno de Oliveira von der State University of Campinas in Brasilien fasste die Sorge so zusammen: 'Ein erheblicher Forschungsstand legt nahe, dass Mikroplastik in Knochengewebe, einschließlich des Markraums, eindringen kann und potenziell metabole Funktionen stört.' Er betont, dass die beobachteten zellulären Dysfunktionen – Entzündungen, verringerte Zellvitalität und veränderte Differenzierung – in Tiermodellen zu unterbrochenem Skelettwachstum geführt haben und daher biologisch plausibel als Mechanismen für schädliche Effekte gelten.
Einordnung in den öffentlichen Gesundheitskontext
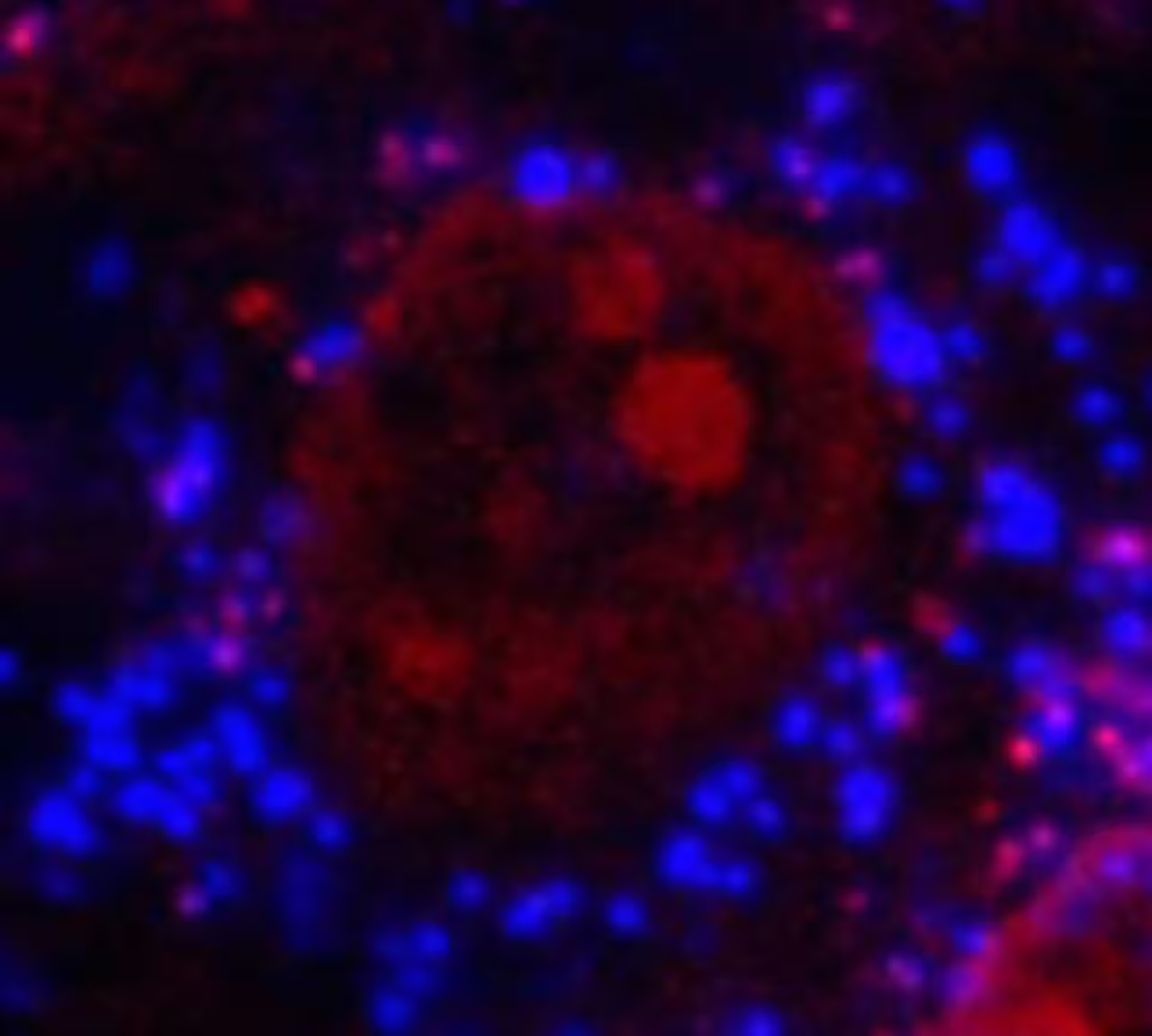
Innenansicht einer MG-63-Knochenzelle vergrößert 400x mit blau hervorgehobenen Mikroplastikkugeln und dem Zellkern in Rot. (Mariana Cassani de Oliveira/LEMON/FCM-UNICAMP)
Die Übertragung von Tier- und In-vitro-Ergebnissen auf konkrete menschliche Krankheitsbilder bleibt herausfordernd. Dennoch steigen in vielen Ländern die Raten von Osteoporose und altersbedingter Knochenbrüchigkeit, angetrieben durch demografische Alterung sowie Lebensstilfaktoren wie Alkoholgebrauch, Rauchen und körperliche Inaktivität. Forscher sehen die Exposition gegenüber Mikroplastik inzwischen als plausiblen zusätzlichen Einflussfaktor an, der in Jahrzehnten intensiver Plastikproduktion bisher nur unzureichend berücksichtigt wurde.
Die derzeitige globale Produktion synthetischer Polymere übersteigt jährlich 400 Millionen Tonnen. Herstellung, Gebrauch und Entsorgung von Kunststoffen tragen erheblich zu Treibhausgasemissionen bei – Schätzungen gehen von rund 1,8 Milliarden Tonnen CO2-Äquivalent pro Jahr aus – und sorgen für persistente Einträge in Umwelt und Nahrungsketten. Diese Produktions- und Abfallströme erzeugen eine fortlaufende Belastung der Umwelt und somit auch eine andauernde menschliche Exposition gegenüber Mikroplastik, was die Frage nach langfristigen gesundheitlichen Folgen umso dringlicher macht.
Aus gesundheitspolitischer Sicht ist wichtig zu betonen, dass Mikroplastik nicht isoliert betrachtet werden darf: Es steht in Verbindung zu anderen Umweltbelastungen wie Luftverschmutzung, chemischer Kontamination und veränderten Ernährungs- und Bewegungsmustern. Die potenziellen additiven oder synergistischen Effekte zwischen diesen Stressoren sind ein kritischer Forschungsbereich, da kombinierte Belastungen andere gesundheitliche Risikoprofile erzeugen können als einzelne Faktoren für sich.
Beschränkungen der aktuellen Datenbasis und Forschungsbedarf
Die Übersichtsarbeit hebt mehrere zentrale Wissenslücken hervor. Quantitative Expositions–Antwort-Beziehungen sind für den Menschen nicht etabliert: Es fehlen belastbare Daten darüber, welche Mengen und Arten von Partikeln im Laufe eines Lebens in Knochengewebe gelangen und welche Konzentrationen klinisch relevante Effekte auslösen. Analytische Schwierigkeiten stellen eine zusätzliche Hürde dar; insbesondere die zuverlässige Identifikation und Messung von Nanoplastik in biologischen Proben ist technisch anspruchsvoll und bedarf standardisierter, validierter Methoden.
Weitere Limitationen sind heterogene Studienprotokolle, unterschiedliche Partikeltypen und -größen in Experimenten sowie oft unrealistisch hohe Dosen in tierexperimentellen Studien, die Umweltexpositionen nicht akkurat nachahmen. Zudem sind populationsbezogene Langzeitdaten rar: Es gibt kaum prospektive Kohortenstudien, die Expositionsdaten mit validen Knochengesundheitsindikatoren wie Knochendichte, Frakturrisiko oder Biomarkern für Knochenstoffwechsel verknüpfen.
Forschungsgruppen fordern koordinierte epidemiologische Studien, langfristige Tierexperimente mit ökologisch relevanten Partikeln und Dosen sowie verbesserte analytische Werkzeuge zur Detektion und Charakterisierung von Nanoplastik in Humanproben. Standardisierte Methoden, offene Protokolle und interdisziplinäre Kooperationen zwischen Toxikologen, Epidemiologen, Materialwissenschaftlern und klinischen Forschern werden als entscheidend angesehen, um belastbare Aussagen zur Relevanz von Mikroplastik für die Knochengesundheit zu treffen.
Zusätzlich werden Forschungsprioritäten identifiziert, die über Nachweisfragen hinausgehen: Untersuchung von Mechanismen auf molekularer Ebene (z. B. Signalwege, Epigenetik), Bewertung von kombinierten Expositionen mit anderen Umweltchemikalien, sowie Modellierung langfristiger gesundheitlicher und ökonomischer Folgen für Gesundheitssysteme. Solche Daten würden politische Maßnahmen und Präventionsstrategien fundierter untermauern.
Praktische Schritte zur Reduktion der Exposition
Solange die Wissenschaft weiter Erkenntnisse generiert, können Einzelpersonen und Institutionen pragmatische Maßnahmen ergreifen, um die Exposition zu minimieren. Dazu gehören das Filtern oder gezielte Behandeln von Trinkwasser zur Entfernung von Partikeln, die Reduktion der Nutzung von Einwegkunststoffen, die bewusste Wahl von Bekleidung aus Naturfasern statt synthetischer Textilien und das Minimieren des Konsums von Lebensmitteln und Getränken in Kunststoffverpackungen.
Institutionelle Maßnahmen sind ebenfalls wirksam: Wasserversorger und kommunale Einrichtungen können in partikelentfernende Technologien investieren, Krankenhäuser und Schulen können Plastikverbrauch reduzieren, und Betriebe können Materialien mit besserer Recyclingfähigkeit oder geringerer Partikelabgabe bevorzugen. Auf politischer Ebene sind Regulierung von Mikroplastikquellen, strengere Vorgaben für Kunststoffadditive und gezielte Förderprogramme für Forschung und alternative Materialien wichtige Hebel.
Für Verbraucher sind einfache Alltagstipps nützlich: Vermeiden Sie das Erhitzen von Lebensmitteln in Kunststoffbehältern, nutzen Sie Glas- oder Edelstahlflaschen, wählen Sie frische oder unverpackte Lebensmittel, und reduzieren Sie die Verwendung von abrasiven Reinigungsmitteln, die synthetische Fasern freisetzen können. Solche Maßnahmen senken nicht nur die direkte Exposition, sondern signalisieren auch eine Nachfrageverschiebung, die nachhaltigere Produktgestaltung fördert.
Fachliche Einschätzung
Dr. Emily Carter, Umwelttoxikologin an einem universitären Forschungsschwerpunkt, kommentierte: 'Die Evidenz, dass Mikroplastik tiefe Gewebe erreicht, wächst. Auch wenn eine direkte Ursache-Wirkung-Beziehung für Osteoporose beim Menschen noch nicht bewiesen ist, sind die im Labor beobachteten zellulären Effekte – Entzündung, gestörte Zellfunktionen und veränderte Differenzierung der Knochenzellen – biologisch plausible Pfade für gesundheitliche Schäden. Priorität sollten bessere Expositionsabschätzungen und standardisierte Detektionsmethoden haben, damit wir von berechtigter Sorge zu konkreter gesundheitsbezogener Anleitung übergehen können.' Diese Einschätzung unterstreicht die Verbindung zwischen methodischer Verbesserung, epidemiologischer Forschung und gesundheitspolitischer Vorsorge.
Fazit
Die Übersichtsarbeit zu 62 Studien betont eine drängende wissenschaftliche und gesundheitspolitische Fragestellung: Mikroplastik ist in Knochen und Knochenmark nachweisbar, und experimentelle Daten zeigen, dass diese Partikel die zellulären Mechanismen stören können, die für gesunden Knochenaufbau und -erhalt verantwortlich sind. Obwohl ein kausaler Zusammenhang beim Menschen bislang nicht eindeutig belegt ist, stützen die Kombination aus steigender Kunststoffproduktion, dokumentierter Gewebeakkumulation und plausiblen biologischen Mechanismen die Forderung nach gezielter Forschung und vorsorglichen Maßnahmen zur Expositionsminderung.
Politiker, Wissenschaftler und die Öffentlichkeit sollten die potenzielle Belastung des Skeletts durch Mikroplastik als legitimes und dringliches Forschungs- und Handlungsfeld betrachten. Kurzfristig sind präventive Schritte auf individueller und institutioneller Ebene sinnvoll; langfristig sind international koordinierte Forschungsvorhaben und Regulierungsmaßnahmen nötig, um die gesundheitlichen Folgen von Mikroplastik umfassend zu bewerten und zu begrenzen.
Quelle: sciencealert

Kommentar hinterlassen