7 Minuten
Memantin verbessert soziales Verhalten bei Teilgruppe von ASD
Ein ursprünglich zur Verlangsamung des kognitiven Abbaus bei Alzheimer entwickeltes Medikament — Memantin — könnte die soziale Kommunikation und Interaktion eines spezifischen Subsets von Kindern mit Autismus-Spektrum-Störung (ASD) verbessern. Eine kürzlich durchgeführte randomisierte klinische Studie unter Leitung von Forschenden des Massachusetts General Hospital und der Harvard University ergab ermutigende Signale, insbesondere wenn das Medikament in höheren Dosen verabreicht und gezielt bei Patientinnen und Patienten mit bestimmten neurochemischen Profilen eingesetzt wurde.
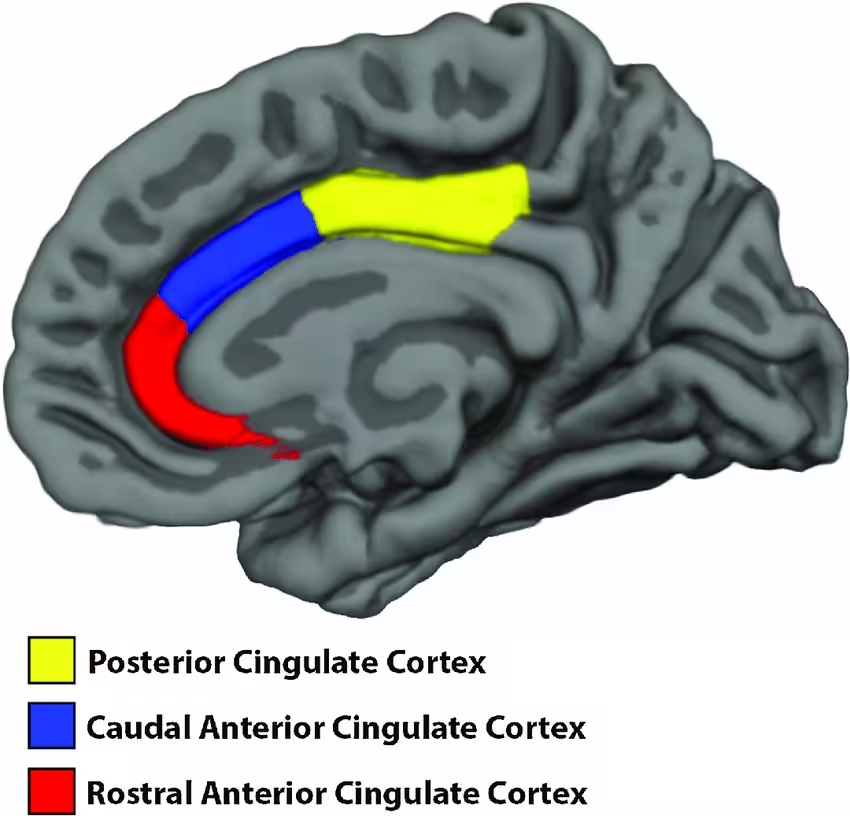
Lage des cingulären Kortex im menschlichen Gehirn. (Overbye et al., Dev. Cog. Neuro., 2019)
Studiendesign und zentrale Ergebnisse
Die Studie rekrutierte 33 Kinder und Jugendliche im Alter von 8 bis 17 Jahren ohne Intelligenzminderung. Die Teilnehmenden wurden randomisiert und doppelblind einer täglichen Behandlung mit 20 mg Memantin oder Placebo über einen Zeitraum von 12 Wochen zugeteilt. Methodisch handelte es sich um ein standardmäßiges randomisiertes, placebo-kontrolliertes Design; die Untersuchenden kombinierten klinische Beobachtungen mit neurowissenschaftlichen Messungen, um Veränderungen in sozialem Verhalten zu erfassen und mögliche biologische Prädiktoren zu analysieren.
Auf Ebene der Gesamtgruppe zeigte sich kein einheitlicher, statistisch eindeutiger Behandlungseffekt — ein Befund, der frühere, heterogenere Studien widerspiegelt. Allerdings trat ein deutliches Muster zutage, als die Forschenden die Teilnehmenden nach Glutamatkonzentrationen in einer sozial relevanten Hirnregion, dem prägenualen anterioren cingulären Kortex (pgACC), stratifizierten. Solche Subgruppenanalysen sind in Studien zu komplexen neuropsychiatrischen Störungen zunehmend wichtig, um pharmakologische Effekte nicht durch biologische Variabilität zu verwässern.
Ungefähr die Hälfte der Kinder zeigte im pgACC erhöhte Glutamatwerte. In dieser Untergruppe berichteten Eltern und Betreuende über statistisch signifikante und klinisch relevante Verbesserungen in Bereichen wie verbale und nonverbale Kommunikation, sozialer Interaktion und allgemeiner sozialer Teilhabe unter Memantin im Vergleich zu Placebo. Dagegen zeigten Kinder ohne erhöhte pgACC-Glutamatwerte keine vergleichbaren Verbesserungen. Diese Differenz deutet darauf hin, dass ein neurochemischer Biomarker helfen kann, diejenigen zu identifizieren, die am ehesten von einer Behandlung profitieren.
Die Autorinnen und Autoren betonen ausdrücklich, dass es sich um vorläufige Befunde handelt: Die Stichprobengröße war klein, die Behandlungsdauer kurz und die Studie ist als Proof-of-Concept zu verstehen. Größere, multizentrische und längerfristige Studien sind erforderlich, um Wirksamkeit, Robustheit der Effekte und Sicherheit im pädiatrischen Bereich endgültig zu bewerten.
Wissenschaftlicher Hintergrund: Glutamat, pgACC und Memantin
Glutamat ist der wichtigste exzitatorische Neurotransmitter im Gehirn und grundlegend für Lernprozesse, synaptische Plastizität und die Bildung von Gedächtnisinhalten. Gleichzeitig kann eine Überaktivität glutamaterger Signalwege zu sogenannter Exzitotoxizität führen, also zu einer schädigenden Übererregung von Neuronen, die neuronale Netzwerke stört und langfristig Funktionseinbußen bewirken kann. In vielen neuropsychiatrischen Erkrankungen, darunter einzelne Subtypen des Autismus, werden veränderte glutamaterge Parameter diskutiert — sowohl auf molekularer Ebene als auch in der Neuroimaging-Bildgebung.
Der prägenuale anteriore cinguläre Kortex (pgACC) ist eine kortikale Region mit hoher Dichte an Glutamatrezeptoren und nimmt eine Schlüsselrolle bei sozialer Kognition, Emotionsverarbeitung, Selbstwahrnehmung und motivationalen Prozessen ein. Änderungen in der Funktion oder Neurochemie des pgACC werden mit Schwierigkeiten bei Empathie, sozialer Belohnungsverarbeitung und der Regulation sozialer Interaktion in Verbindung gebracht — Domänen, die häufig bei ASD betroffen sind. Deshalb ist der pgACC eine plausibel relevante Zielstruktur für interventionsorientierte Forschung.
Memantin wirkt vornehmlich als NMDA-Rezeptor-Antagonist. Es handelt sich um einen niedrig- bis mittelaffinen, spannungsabhängigen und unkompetitiven Blocker, der exzessive NMDA-getriebene Aktivität dämpft, ohne physiologische glutamaterge Übertragungen grundlegend zu unterdrücken. Diese pharmakodynamischen Eigenschaften machen Memantin in der Neurologie seit langem interessant: Bei neurodegenerativen Erkrankungen wie der Alzheimer-Krankheit kann Memantin pathologisch gesteigerte glutamaterge Signalübertragung abschwächen und so das Fortschreiten bestimmter Symptome verzögern. Die neue Studie legt nahe, dass ein vergleichbarer Mechanismus — das Reduzieren übermäßiger glutamaterger Aktivität in spezifischen Netzwerken — bei Kindern mit erhöhtem pgACC-Glutamat soziale Symptome verbessern könnte.
In der vorliegenden Arbeit wurden die Glutamatwerte mittels bildgebender Verfahren quantifiziert, die neurotransmitterbezogene Konzentrationen messbar machen — typischerweise durch protonenbasierte Magnetresonanzspektroskopie (1H-MRS). MRS erlaubt die nicht-invasive Abschätzung regionaler Metabolitkonzentrationen im Gehirn und ist damit ein geeignetes Werkzeug, um neurochemische Subgruppen zu identifizieren. Allerdings ist MRS technisch anspruchsvoll: Die räumliche Auflösung ist begrenzt, Messwerte sind sensitiv gegenüber Artefakten, und die absolute Quantifizierung erfordert sorgfältige Kalibrierung und Standardisierung zwischen Zentren. Dennoch bietet MRS heute eine praktikable Option als biomarkergestützte Methode für personalisierte Interventionen.
Implikationen und nächste Schritte
Die Ergebnisse dieser Studie haben mehrere wichtige Implikationen für klinische Forschung und die Entwicklung präzisionsmedizinischer Ansätze bei Autismus:
- Heterogenität zählt: ASD ist biologisch und klinisch heterogen. Behandlungen, die bei einer bestimmten biologischen Subgruppe wirken, können in unselektierten Kohorten untergehen. Früher durchgeführte Studien, die ASD als eine homogene Entität behandelten, haben möglicherweise subgroup-spezifische Effekte übersehen.
- Biomarker-gestützte Therapie: Die Messung von Gehirn-Glutamat könnte als prädiktiver Biomarker dienen, um Therapieentscheidungen zu individualisieren. Solche Tests können unnötige Expositionen vermeiden und die Chancen erhöhen, dass diejenigen behandelt werden, die am meisten profitieren.
Für die folgenden Forschungsphasen empfehlen die Autorinnen und Autoren größere, multizentrische Studien mit längerer Nachbeobachtung, erweiterten Altersgruppen und strengem Sicherheitsmonitoring. Wichtig sind zudem robuste klinische Endpunkte, standardisierte Verhaltensmessungen, objektivierbare neurophysiologische Marker und, wenn möglich, mechanistische Nebenstudien (z. B. Messung von Signalübertragungsparametern, funktionelle Konnektivität oder Longitudinaluntersuchungen der Neurochemie).
Weitere Aspekte, die in zukünftigen Studien berücksichtigt werden sollten, sind:
- Pharmakokinetik und Dosisfindung im Kindes- und Jugendalter: Kinder metabolisieren Medikamente anders als Erwachsene, und die sichere, wirksame Dosis kann variieren. Längere Follow-up-Intervalle sind notwendig, um mögliche Einflüsse auf neurodevelopmentale Prozesse zu dokumentieren.
- Sicherheitsprofil und Nebenwirkungen: Obwohl Memantin bei Erwachsenen ein bekanntes Sicherheitsprofil hat, müssen kurz- und langfristige Nebenwirkungen im pädiatrischen Kontext gezielt untersucht werden — etwa Effekte auf Schlaf, Verhalten, Wachstumsparameter oder Interaktionen mit anderen zentral wirksamen Medikamenten.
- Validierung und Standardisierung des Biomarkers: Die Nutzung von MRS als Screening-Werkzeug erfordert eine hohe Reproduzierbarkeit und Vergleichbarkeit zwischen Studienzentren. Validierte Protokolle, normative Referenzdaten und Qualitätskontrollstandards sind Voraussetzung für breitere klinische Anwendung.
- Ethik und Zugänglichkeit: Biomarker-geleitete Therapien sollten so implementiert werden, dass Ungleichheiten in der Gesundheitsversorgung nicht verstärkt werden. Kosten, Verfügbarkeit von MRS und die Interpretation von Befunden müssen in einen gerechten Versorgungsansatz integriert werden.
Wenn sich die Befunde in größeren, methodisch robusten Studien bestätigen, könnte Memantin für einen substanziellen Anteil von Kindern mit ASD und erhöhtem pgACC-Glutamat zu einer gezielten Behandlungsoption werden. Solch ein Ansatz würde es ermöglichen, Therapie effizienter und schonender zu gestalten — indem nur diejenigen exponiert werden, die mit hoher Wahrscheinlichkeit profitieren — und könnte gleichzeitig Forschungserkenntnisse zur Pathophysiologie sozialer Beeinträchtigungen bei Autismus liefern.
Fazit
Eine kleine, gezielt angelegte klinische Studie deutet darauf hin, dass Memantin die soziale Kommunikation und Teilhabe bei Kindern mit ASD verbessern kann, sofern im prägenualen anterioren cingulären Kortex erhöhte Glutamatwerte vorliegen. Die Ergebnisse unterstreichen die Bedeutung biomarkergetriebener Forschungsansätze in der Autismusforschung und betonen die biologische Variabilität dieser Störung. Bevor Memantin jedoch als therapeutische Option für pädiatrische ASD-Populationen empfohlen werden kann, sind größere, longitudinale und methodisch stringente Studien nötig, die Wirksamkeit, Sicherheit und Langzeitfolgen belastbar abklären.
Quelle: sciencealert


Kommentar hinterlassen