10 Minuten
Forschende berichten von einer ersten Stammzelltransplantation beim Menschen, die offenbar bei einigen älteren Patientinnen und Patienten mit trockener altersbedingter Makuladegeneration (AMD) die Zentralsehschärfe wiederherzustellen scheint. Frühphasige klinische Daten deuten darauf hin, dass das Verfahren sicher ist und bei den am stärksten betroffenen Studienteilnehmenden bedeutsame Sehverbesserungen brachte. Diese vorläufigen Ergebnisse haben die Forscher veranlasst, zusätzliche Studien mit höheren Zellzahlen durchzuführen, um Sicherheit und Wirksamkeit weiter zu prüfen.
Warum die Zentralvision bei trockener AMD nachlässt — und warum das wichtig ist
Die altersbedingte Makuladegeneration ist die häufigste Ursache für irreversiblen zentralen Sehverlust im höheren Lebensalter. Die Makula ist der kleine, zentrale Bereich der Netzhaut, der für scharfes Sehen zuständig ist und Funktionen wie Lesen, Gesichtserkennung oder das sichere Autofahren ermöglicht. Bei der trockenen Form der AMD, die etwa 80 % aller Fälle ausmacht, lagern sich unter der retinalen Pigmentepithelschicht (RPE) kleinste Ablagerungen aus Lipiden und Proteinen, sogenannte Drusen, ab. Diese Ablagerungen stören über die Jahre die Funktion der RPE-Zellen — des Stützgewebes, das die lichtempfindlichen Photorezeptoren ernährt, entsorgt und stabilisiert. Durch den fortschreitenden Verlust dieser RPE-Zellen kommt es zu einer fortschreitenden Schädigung der Photorezeptoren und zu einer allmählichen Trübung oder Ausdünnung des zentralen Gesichtsfeldes, die als zentrale Skotome oder Verschwommensehen wahrgenommen wird.
Die klinische Bedeutung der RPE liegt nicht nur in ihrer Rolle als metabolische Unterstützung der Photorezeptoren, sondern auch in ihrer Funktion bei der Phagozytose von abgestoßenen Photorezeptorensegmenten, bei der Aufrechterhaltung der Blut-Retina-Schranke und bei der Regulation lokaler Entzündungs- und Komplementwege. Schäden an der RPE können daher multiple pathophysiologische Kaskaden anstoßen — von oxidativem Stress bis zur chronischen lokalen Entzündung — und so die Krankheit beschleunigen. Epidemiologisch führt die trockene AMD bei vielen Betroffenen zu zunehmender Abhängigkeit von Sehhilfen, zu Einschränkungen der Mobilität und zu einer verminderten Lebensqualität; in der Bevölkerung ist sie eine der vordringlichen Ursachen für altersbedingte Sehbehinderung.
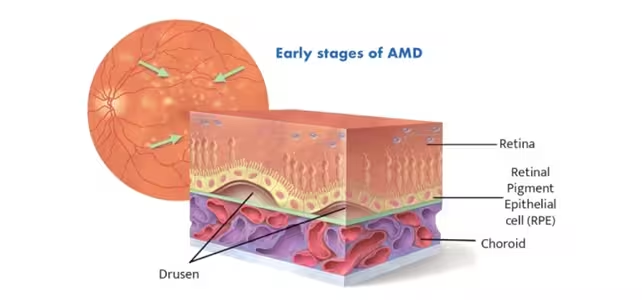
Diagramm, das frühe Stadien der trockenen Makuladegeneration zeigt, verursacht durch Ablagerungen aus Fetten und Proteinen (Drusen) unter der RPE.
Was in der neuen Studie getestet wurde und wie das Verfahren funktioniert
Die veröffentlichte Phase-1/2a-Studie untersuchte die Transplantation von RPE-Zellen, die aus adulten Stammzellen gewonnen und von einer Augenbank bereitgestellt wurden. Ziel dieser frühen Studienphase war primär die Prüfung der Sicherheit und eine erste Einschätzung der Wirksamkeit — ein direkter Vergleich mit etablierten Therapien war zu diesem Zeitpunkt nicht vorgesehen. Für die Studie wurden 18 potenzielle Teilnehmende gescreent; eingeschlossen wurden schließlich sechs Freiwillige im Alter von 71 bis 86 Jahren, die eine fortgeschrittene trockene AMD in einem Auge aufwiesen. Solche frühen Humanstudien sind darauf ausgelegt, mögliche Risiken zu identifizieren und erste Signale für einen therapeutischen Nutzen zu erfassen, um darauf aufbauend größere randomisierte Studien planen zu können.
Applikation und Dosierung
Jede Probandin bzw. jeder Proband erhielt einmalig eine vergleichsweise geringe Dosis von 50.000 RPE-Stammzellen, die subretinal in die superior-temporale Makula des schlechter sehenden Auges injiziert wurden. Die subretinale Verabreichung zielt darauf ab, die Zellen unmittelbar in das mikroumfeld der beschädigten RPE-Schicht zu bringen, damit sie dort die geschädigten RPE-Funktionen übernehmen oder wiederherstellen können. Operativ erfolgt der Eingriff in der Regel mithilfe einer Pars-plana-Vitrektomie, gefolgt von einer vorsichtigen subretinalen Injektion zur Platzierung der Zellen in der Makula; Ziel ist es, die Mikroumgebung für die Photorezeptoren zu stabilisieren und die lokale Homöostase wiederherzustellen. Die Idee hinter der RPE-Transplantation ist, verloren gegangene oder dysfunktionale RPE zu ersetzen, damit die Photorezeptoren wieder ausreichend ernährt, unterstützt und vor schädlichen Stoffwechselprodukten geschützt werden.
Vorläufige Laborstudien und Sicherheitsprüfungen
Präklinische Laboruntersuchungen hatten zuvor gezeigt, dass die transplantierten Zellen ihre retinale Identität beibehalten und in Zellkultur sowie in Tiermodellen typische RPE-Marker exprimieren. Zudem ergaben GLP-konforme Toxizitätsstudien keine Hinweise auf Tumorbildung oder systemische Toxizität, was die Grundlage für die Zulassung humaner Studien bildete. Solche Studien umfassen in der Regel sowohl In-vitro-Analysen (Genexpressionsprofile, Marker der Differenzierung) als auch In-vivo-Untersuchungen in Tiermodellen zur Beurteilung von Biodistribution, Tumorigenität und lokalen Reaktionen. Während der klinischen Studie wurden die Teilnehmenden engmaschig überwacht — mit regelmäßigen ophthalmologischen Kontrollen, Bildgebung (OCT, Fundusfotografie), Laborparametern und Assessments zur Abwehrreaktion — um mögliche Immunreaktionen, Neoplasien oder typische Komplikationen einer Netzhautchirurgie frühzeitig zu erkennen.
Wesentliche Ergebnisse: Sicherheit zuerst — und überraschende Sehverbesserungen
Die Studie erreichte ihre primären Sicherheitsendpunkte: Es traten keine unerwünschten Ereignisse auf, die direkt auf die implantierten Stammzellen zurückgeführt werden konnten. Insbesondere gab es keine Hinweise auf Tumorbildung und keine eindeutigen Befunde, die eine zellvermittelte immunologische Abstoßungsreaktion belegten. Einige Teilnehmende erlitten erwartbare chirurgische Komplikationen, die in der Regel als behandelbar beschrieben werden — solche Komplikationen können beispielsweise postoperativ erhöhte Augeninnendruckwerte, vorübergehende Entzündungszeichen, vitreale Einblutungen oder seltenere Netzhautkomplikationen umfassen — diese Ereignisse wurden jedoch als handhabbar eingestuft und nicht mit dem Zellprodukt selbst in Verbindung gebracht.
Auf der Wirksamkeitsseite überraschten die Forschenden mit Verbesserungen der Sehschärfe, die auf das behandelte Auge beschränkt waren. Drei Teilnehmende mit der schlechtesten Ausgangssehschärfe (ungefähr 20/200 bis 20/800) gewannen im Mittel 21 Buchstaben auf dem Sehzeichenblatt (entspricht etwa vier Linien) ein Jahr nach der Injektion. Die drei anderen Studienteilnehmenden, die mit besserer Ausgangssehschärfe (etwa 20/70 bis 20/200) starteten, zeigten kleinere Verbesserungen. Dass die Funktionsverbesserung unilateral — nur im Auge mit der Zelltransplantation — auftrat, stärkt die Hypothese, dass die Zellen selbst zu den beobachteten Seheffekten beigetragen haben, und reduziert die Wahrscheinlichkeit, dass systemische oder andere interventionelle Faktoren allein Verantwortliche sind.
"Obwohl wir mit den Sicherheitsdaten zufrieden waren, war der aufregende Teil, dass sich ihr Sehen ebenfalls verbesserte", erklärte Rajesh Rao, Ärztlicher Wissenschaftler und Augenarzt an der Michigan Medicine. "Wir waren überrascht von dem Ausmaß der Sehverbesserung bei den am stärksten betroffenen Patientinnen und Patienten, die die aus adulten Stammzellen gewonnenen RPE-Transplantate erhalten haben. Eine solche Steigerung der Sehschärfe wurde in dieser Patientengruppe mit fortgeschrittener trockener AMD bisher nicht beobachtet."
Was das für Patientinnen und Patienten bedeutet und die nächsten Forschungsschritte
Die Befunde sind vielversprechend, aber vorläufig. Die sehr kleine Studienpopulation — sechs Teilnehmende mit einer niedrigen Startdosis — macht deutlich, dass größere, randomisierte und kontrollierte Studien notwendig sind, um den tatsächlichen Nutzen zu bestätigen, die Dauerhaftigkeit der Effekte zu messen und die Ergebnisse mit bestehenden oder in Entwicklung befindlichen Therapien zu vergleichen. Wichtige Endpunkte künftiger Studien werden standardisierte Messungen der bestkorrigierten Sehschärfe (BCVA), niedrig-luminante Sehtests, Mikroperimetrie zur Kartierung der retinalen Sensitivität, OCT-basierte morphologische Marker sowie patientenberichtete Outcomes zur Lebensqualität sein. Ebenfalls relevant sind Langzeitdaten zur Persistenz der transplantierten Zellen, zur Integration in das umliegende Gewebe und zur Stabilität der funktionellen Verbesserungen.
Die Studie wird weiterhin Gruppen beobachten, die höhere Zellzahlen erhalten — 150.000 und 250.000 Zellen — um zu ermitteln, ob eine Dosiseskalation die Sicherheit bewahrt und gleichzeitig die Wirksamkeit steigert. Sollte sich zeigen, dass höhere Dosen sicher sind und gleiche oder größere Seherholungen ermöglichen, würden Forschende Phase-3-Studien planen, die das neue Verfahren gegen die derzeitige Standardversorgung prüfen. Selbst bei positiver Wirksamkeit wären aber noch mehrere Jahre nötig, bis Zulassungsverfahren, die Skalierung der Herstellung (Good Manufacturing Practice, GMP), Lieferketten und der breite klinische Zugang etabliert sind.
Verwandte Technologien und klinischer Kontext
RPE-Transplantate aus Stammzellen sind Teil eines wachsenden Portfolios regenerativer Ansätze, die auf Erkrankungen der Netzhaut zielen. Dazu zählen Gentherapien, die molekulare Defekte korrigieren oder modifizieren, zellbasierte Schichtimplantate (RPE-Patches), bioengineerte Zellverbände, sowie neuartige Arzneimittelexpositionssysteme und intravitreale Wirkstoffabgabetechnologien, die das Fortschreiten der Degeneration verlangsamen sollen. Parallel entwickeln sich optische Prothesen, Neuroprotektion und Hilfsmittel für niedriges Sehvermögen weiter, die das Ziel verfolgen, verbliebene Sehleistung zu erhalten oder bei weiter fortgeschrittener Erkrankung funktionale Hilfen zu bieten.
Für Menschen mit trockener AMD — die bislang nur begrenzte therapeutische Optionen jenseits von Lebensstilmaßnahmen, Vitaminpräparaten in spezifischen Präparaten und Low-Vision-Hilfen haben — könnte ein sicheres und wirksames RPE-Transplantat einen Paradigmenwechsel bedeuten: weg von rein symptomatischer Milderung hin zu echter teilweiser Wiederherstellung retinaler Funktion. Darüber hinaus birgt die Kombination von Zelltherapien mit begleitenden Ansätzen (z. B. gezielter Immunmodulation, complement-inhibitorischen Strategien oder Gerüstmaterialien) das Potenzial für synergistische Effekte, die sowohl die Überlebensrate der transplantierten Zellen als auch ihre funktionelle Integration verbessern könnten.
Experteneinschätzung
"Eine gezielte RPE-Transplantation adressiert einen spezifischen Schwachpunkt bei der trockenen AMD: den Verlust unterstützender Pigmentepithelzellen", sagt Dr. Elena Morales, Netzhautchirurgin und translationale Wissenschaftlerin. "Wenn es gelingt, diese Zellen zuverlässig zu ersetzen, ohne Immunprobleme oder Tumorrisiken auszulösen, könnten sich daraus erhebliche Vorteile für die Photorezeptoren ergeben. Die nächsten Hürden sind die Reproduzierbarkeit der Ergebnisse und die langfristige Integration der transplantierten Zellverbände in die komplexe Architektur der Netzhaut."
Insgesamt signalisiert diese erste klinische Studie, dass zellbasierte Therapien ein realistischer Weg sind, um strukturelle Defekte der Makula direkt anzugehen. Entscheidend wird sein, ob größere, methodisch robuste Studien die initialen Signale bestätigen, wie gut die Effekte über Jahre anhalten und welche patientenspezifischen Faktoren (z. B. Alter, Komorbiditäten, Stadium der AMD) das Ansprechen vorhersagen. Während die Forschung voranschreitet, bleibt eine enge Zusammenarbeit zwischen Klinikerinnen und Klinikern, Regulierungsbehörden, Herstellern und Patienten essenziell, um sicherzustellen, dass Therapieentwicklung, Sicherheitsüberwachung und ethische Standards Hand in Hand gehen.
Quelle: sciencealert

Kommentar hinterlassen