6 Minuten
Forschende an der University of California, Irvine berichten, dass ein natürlicher Antioxidans aus grünem Tee, kombiniert mit einer gebräuchlichen Form von Vitamin B3, ein zentrales zelluläres Energymolekül in Neuronen wiederherstellen und die Abfallbeseitigungsmechanismen des Gehirns stimulieren kann. In im Labor gezüchteten Mausneuronen erhöhte diese Kombination die Guanosintriphosphat (GTP)-Spiegel, belebte autophagiebezogene Reinigungsfunktionen und reduzierte Amyloid‑Beta‑Aggregate — Kennzeichen, die mit der Alzheimer‑Krankheit assoziiert werden. Da beide Verbindungen über Lebensmittel und als zugelassene Nahrungsergänzungsmittel verfügbar sind, deuten die Ergebnisse auf einen plausiblen, risikoarmen Weg für weitergehende therapeutische Entwicklungen hin.
Wissenschaftlicher Hintergrund: EGCG, Nicotinamid und zelluläre Energie
Epigallocatechingallat (EGCG) ist ein in grünem Tee reichlich vorhandenes Polyphenol, dem antioxidative und neuroprotektive Eigenschaften zugeschrieben werden. Nicotinamid ist eine Form von Vitamin B3 (ein Metabolit von Niacin), die in Getreide, Fisch, Nüssen, Hülsenfrüchten und Eiern vorkommt und durch normalen Zellstoffwechsel gebildet wird. Das UC Irvine-Team untersuchte diese beiden Moleküle gemeinsam, um zu prüfen, ob sie intrazelluläre Nukleotid-Pools beeinflussen können — speziell Guanosintriphosphat (GTP), ein weniger untersuchter Energieträger, der wichtige neuronale Prozesse unterstützt.
GTP ist an zahlreichen zellulären Funktionen beteiligt, darunter Mikrotubulusdynamik, intrazellulärer Transport und Autophagie — das System der Zelle zur Abbau und Wiederverwertung beschädigter Proteine und Organellen. Frühere Forschungen haben sinkende neuronale Energiestatus und gestörte Proteostase mit Altern und neurodegenerativen Erkrankungen in Verbindung gebracht. Die neuen Experimente identifizieren den GTP‑Abfall als potenziellen mechanistischen Beitrag zur altersbedingten Ansammlung toxischer Proteinaggregate.
Methoden und zentrale experimentelle Befunde
In-vitro-Experimente verwendeten kultivierte kortikale Mausneuronen, die EGCG und Nicotinamid einzeln und in Kombination ausgesetzt wurden. Die Forschenden maßen intrazelluläre GTP-Spiegel, Marker der Autophagie und das Vorkommen von Amyloid‑Beta‑Aggregaten. Zudem wurden neuronale Marker für alterungsbedingte Schäden bewertet.
Die kombinierte Behandlung führte zu einem messbaren Anstieg von GTP gegenüber Kontrollen, und Neuronen mit höheren GTP-Werten zeigten einen verbesserten autophagischen Fluss — ein Hinweis darauf, dass die Recycling‑Maschinerie effektiver arbeitete. Wichtig ist, dass behandelte Zellen eine verringerte Amyloid‑Beta‑Akkumulation und eine teilweise Umkehr von Alterungsmarkern zeigten. Diese Ergebnisse legen nahe, dass die Wiederherstellung des Nukleotid‑Energiebalances Neuronen befähigen kann, toxische Proteine zu entfernen.
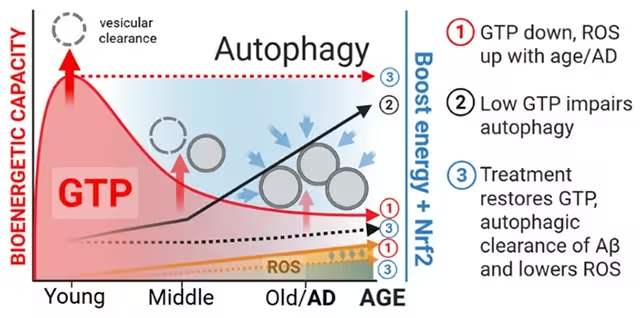
Die Studie betont, dass die beobachteten Effekte am stärksten waren, wenn EGCG und Nicotinamid gemeinsam appliziert wurden, was auf Synergie hindeutet: Die antioxidative und signalgebende Wirkung von EGCG könnte die Rolle von Nicotinamid in der Nukleotid‑ und NAD+-Metabolik ergänzen und gemeinsam die GTP‑Wiederherstellung unterstützen.
Implikationen für Alzheimer‑Forschung und Therapieentwicklung
Die Arbeit hebt GTP als einen bislang unterschätzten Treiber neuronaler Haushaltsfunktionen hervor. Wenn GTP‑Erschöpfung zur langsamen Ansammlung fehlgefalteter Proteine im alternden Gehirn beiträgt, könnten Therapien, die die Nukleotid‑Balance wiederherstellen, die nachgelagerte Pathologie verlangsamen oder verhindern — einschließlich der Amyloidaggregation, die mit Alzheimer in Verbindung steht.
Obwohl EGCG und Nicotinamid über Ernährung und Ergänzungsmittel zugänglich sind, warnen die Autoren und andere Expertinnen und Experten, dass diese Ergebnisse aus in‑vitro‑Modellen mit Maus‑Zellen stammen. Die Übertragung solcher Befunde auf den Menschen erfordert sorgfältige Dosisoptimierung, pharmakokinetische Untersuchungen und kontrollierte klinische Studien, um Sicherheit und Wirksamkeit bei der Prävention oder Modifikation neurodegenerativer Erkrankungen zu bestimmen.
Frühere epidemiologische Arbeiten haben regelmäßigen Grüntee‑Konsum mit weniger Weißsubstanzläsionen und einem geringeren Demenzrisiko in Verbindung gebracht, wobei kausale Zusammenhänge bislang unbewiesen sind. Nicotinamid und verwandte NAD+-Vorläufer zeigten neuroprotektive Effekte in Schlaganfallmodellen und anderen Studien zur Neurodegeneration. Diese neue mechanistische Verbindung zu GTP bietet eine plausible biochemische Erklärung für einige dieser Beobachtungen und liefert ein konkretes biochemisches Ziel für weitere Forschung.
Expertinnen‑ und Experteneinschätzung
Dr. Amina Patel, Professorin für Neurobiologie am Institute for Brain Health (fiktional), kommentiert: "Die Ergebnisse der UC Irvine sind überzeugend, weil sie die Aufmerksamkeit auf den Nukleotid‑Energiestatus — konkret GTP — als veränderbaren Faktor in der neuronalen Erhaltung lenken. Wir müssen prüfen, ob vergleichbare GTP‑Defizite in menschlichen Neuronen im Alter und bei Alzheimer‑Gehirnen auftreten und ob diätetische oder supplementäre Ansätze therapeutisch wirksame Konzentrationen im menschlichen Zentralnervensystem erreichen können."
Dr. Patel fügt hinzu: "Erfreulich ist, dass die Verbindungen in vielen Kontexten bereits hinsichtlich ihrer Sicherheit charakterisiert sind, doch die klinische Translation wird rigorose Studien erfordern. Diese Studie liefert uns eine klare biochemische Hypothese zum Testen."
Grenzen, Sicherheit und nächste Schritte
Wichtige Einschränkungen, die zu beachten sind:
- Die Experimente wurden in kultivierten Mausneuronen durchgeführt, nicht in lebenden Tieren oder Menschen. Zelluläre Reaktionen können in intaktem Hirngewebe deutlich abweichen.
- Effektive Konzentrationen in vitro sind beim Menschen möglicherweise nicht erreichbar oder ohne Formulierungsänderungen und Lieferstrategien, die die Gehirn‑Bioverfügbarkeit verbessern, nicht sicher.
- Langfristige Effekte, Wechselwirkungen mit anderen Medikamenten und potenzielle Off‑Target‑Konsequenzen einer chronischen Manipulation von Nukleotid‑Pools sind unbekannt.
Geplante nächste Schritte umfassen die Validierung der GTP‑Antwort in Tiermodellen des Alterns und der Alzheimer‑Erkrankung, die Aufklärung der genauen biochemischen Pfade, durch die EGCG und Nicotinamid GTP steigern, sowie die Ausarbeitung translationaler Studien, die Dosierung, Blut‑Hirn‑Schranken‑Penetration und Sicherheit bei älteren Erwachsenen adressieren.
Verwandte Technologien und Forschungsrichtungen
- Nutraceutical‑Formulierungen und Prodrugs, die die ZNS‑Verabreichung von EGCG oder Nicotinamidderivaten verbessern.
- Biomarker zur Überwachung neuronaler GTP‑Spiegel oder autophagischer Aktivität in vivo.
- Kombinationsstrategien, die metabolische Unterstützung mit Anti‑Amyloid‑ oder Anti‑Tau‑Therapeutika koppeln.
Fazit
Die Studie der UC Irvine identifiziert einen vielversprechenden biochemischen Ansatz — die Wiederherstellung neuronaler GTP‑Spiegel mittels eines Polyphenols aus grünem Tee (EGCG) zusammen mit Nicotinamid — der Autophagie reaktiviert und die Amyloid‑Beta‑Akkumulation in kultivierten Mausneuronen reduziert. Die Ergebnisse beleuchten einen möglichen Mechanismus, der Ernährung, supplementierbare Metabolite und Proteostase im Gehirn verbindet, und stützen weiterführende präklinische und klinische Forschung. Trotz ermutigender Ergebnisse sind diese Befunde vorläufig: Kontrollierte Tierstudien und Studien am Menschen sind erforderlich, um zu klären, ob dieser Ansatz in sichere, wirksame Präventions‑ oder Behandlungsstrategien für die Alzheimer‑Erkrankung übertragbar ist.
Quelle: sciencealert


Kommentar hinterlassen