8 Minuten
Zusammenfassung und Hauptergebnis
Ein internationales Forschungsteam hat gezeigt, dass das Erhöhen der Aktivität von Mitochondrien — den zellulären „Kraftwerken“ — Gedächtnis- und motorische Defizite bei Mäusen, die so verändert wurden, dass sie demenzähnliche Symptome zeigen, rückgängig machen kann. In Nature Neuroscience veröffentlicht, verwendet die Studie ein Forschungswerkzeug namens mitoDREADD-Gs, um gezielt die mitochondriale Funktion in Neuronen zu stimulieren, und liefert damit Belege dafür, dass eine beeinträchtigte mitochondriale Aktivität eine treibende Ursache neurodegenerativer Symptome sein kann und nicht nur eine nachgelagerte Folge.
Die Experimente zeigen nicht nur Korrelation, sondern Kausalität: Wenn die mitochondriale Aktivität chemisch gesteigert wird, verbessern sich kognitive und motorische Beeinträchtigungen; wenn die mitochondriale Funktion pharmakologisch gehemmt und dann mit demselben Werkzeug reaktiviert wird, kehren die Defizite zurück und können erneut behoben werden. Diese Ergebnisse machen Mitochondrien zu einem vielversprechenden Ziel für künftige Therapien gegen Alzheimer und verwandte neurodegenerative Erkrankungen.
Wissenschaftlicher Hintergrund: Mitochondrien und Neurodegeneration
Mitochondrien sind intrazelluläre Organellen, die für die Produktion von Adenosintriphosphat (ATP) verantwortlich sind, der Energiewährung, die zelluläre Prozesse antreibt. In Neuronen, die einen hohen Energiebedarf haben, ist die Leistung der Mitochondrien besonders wichtig für synaptische Signalübertragung, Plastizität und Überleben. In den letzten zehn Jahren haben viele Studien mitochondriale Dysfunktion mit Alterung und neurodegenerativen Erkrankungen wie Alzheimer und Parkinson in Verbindung gebracht, aber eine wichtige Frage blieb: Ist das Versagen der Mitochondrien eine Ursache für neuronalen Verlust und kognitiven Abbau oder eine sekundäre Folge anderer pathologischer Prozesse?
Indem das Team ein experimentelles System entwickelte, mit dem man die mitochondriale Aktivität in lebendem Nervengewebe an- und ausschalten kann, wurde dieses Ursache-Wirkungs-Problem direkt adressiert. Giovanni Marsicano, Neurowissenschaftler bei INSERM, erklärt, dass die Arbeit die erste klare Demonstration sei, die mitochondriale Beeinträchtigung mit Verhaltenssymptomen der Neurodegeneration verknüpft und nahelegt, dass Energiemangel in Neuronen die Kaskade einleiten kann, die zur Degeneration führt.
Details des Experiments: mitoDREADD-Gs, CNO, Mausmodelle und menschliche Zellen
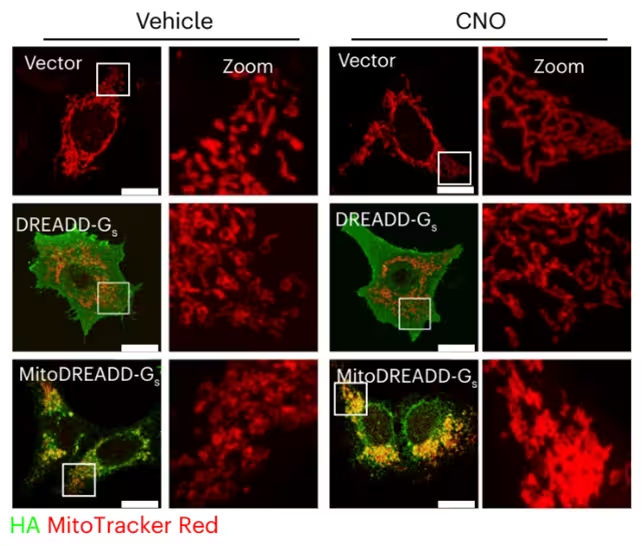
Der zentrale experimentelle Fortschritt ist mitoDREADD-Gs, ein genetisch kodierter Aktivator, der auf Mitochondrien ausgerichtet ist und auf ein Designer-Drug, Clozapin-N-oxid (CNO), reagiert. Im Prinzip wirkt CNO wie ein Zündschlüssel: Die Bindung an mitoDREADD-Gs erhöht mitochondriales Signaling und stimuliert die ATP-Produktion in Zellen, die den Aktivator exprimieren. Bei CNO-Behandlung wurde die mitochondriale Aktivität (in Rot) gesteigert (rechte Panels). (Zottola et al., Nat. Neurosci., 2025)
Die Forschenden führten mitoDREADD-Gs in die Neuronen von Mäusen ein, die genetisch so verändert wurden, dass sie zentrale Merkmale der Demenz nachbilden. Sie testeten das System auch in im Labor kultivierten menschlichen Zellen. In beiden Systemen verbesserte die vorübergehende Aktivierung der mitochondrialen Aktivität die Gedächtnisleistung in Verhaltensassays und linderte motorische Defizite. Um die Reversibilität zu prüfen, nutzte das Team Pharmaka, um die mitochondriale Aktivität zu verringern; die anschließende Anwendung von CNO zur Aktivierung von mitoDREADD-Gs stellte die Funktion wieder her und untermauerte die Interpretation, dass die mitochondriale Beeinträchtigung für die beobachteten Symptome verantwortlich war und nicht nur zufälliger Schaden.
Die Experimente kombinierten Molekularbiologie, Lebendzellbildgebung, Elektrophysiologie und Verhaltenstests, um die zelluläre Bioenergetik mit Ergebnissen auf Organismus-Ebene zu verknüpfen. Wichtig ist, dass mitoDREADD-Gs ein Forschungswerkzeug und kein therapeutisches Produkt ist. Seine Fähigkeit, zeitlich und örtlich zu zeigen, wann und wo mitochondriale Aktivierung die neuronale Funktion beeinflusst, liefert jedoch eine Blaupause zur Identifikation pharmakologisch angreifbarer molekularer Ziele.
Auswirkungen auf Alzheimer und zukünftige therapeutische Strategien
Die Studie schlägt einen neuen Ansatz für die Entwicklung von Behandlungen neurodegenerativer Erkrankungen vor: die Wiederherstellung oder Aufrechterhaltung der mitochondriellen Leistungsfähigkeit in besonders anfälligen Neuronen. Étienne Hébert Chatelain von der Université de Moncton weist darauf hin, dass das Werkzeug helfen kann, die molekularen und zellulären Pfade zu kartieren, die vom Energiemangel zur neuronalen Funktionsstörung führen, und damit die Suche nach wirksamen therapeutischen Zielen zu leiten. Wenn eine beeinträchtigte mitochondriale Aktivität in manchen Formen der Demenz ein frühzeitiger Auslöser ist, könnten pharmakologische Strategien, die den mitochondrialen Stoffwechsel verbessern oder seinen Abfall verhindern, Symptome verlangsamen oder umkehren.
Die Forschenden betonen mehrere Vorbehalte. Demenz ist heterogen: viele genetische, metabolische, vaskuläre und Umwelt-Risikofaktoren tragen zum Ausbruch und Fortschreiten der Krankheit bei. Was in einem bestimmten Mausmodell oder einem kontrollierten Zellkultursystem wirkt, überträgt sich möglicherweise nicht direkt auf das komplexe menschliche Gehirn. Langfristige Effekte müssen ebenfalls sorgfältig untersucht werden: Chronische Stimulierung der mitochondrialen Funktion könnte unvorhergesehene Folgen haben, einschließlich veränderter zellulärer Signalwege, oxidativem Stress oder metabolischer Dysbalance. Luigi Bellocchio von INSERM hebt die nächsten experimentellen Prioritäten hervor: die Messung der Effekte einer längerfristigen mitochondrialen Stimulation auf neuronales Überleben, Krankheitsverlauf und ob frühe Intervention neuronalem Verlust verzögern oder verhindern kann.
Verwandte Technologien und ergänzende Ansätze
Diese Arbeit steht neben anderen mitochondrienfokussierten Strategien, die untersucht werden, darunter kleine Moleküle, die die mitochondriale Biogenese fördern, Antioxidantien, die reaktive Sauerstoffspezies reduzieren, und Gentherapien, die defekte mitochondriale DNA korrigieren. Die Kombination einer mitochondrialen Aktivierung mit Behandlungen, die auf Amyloid, Tau, Entzündung oder vaskuläre Gesundheit abzielen, könnte erforderlich sein, um die multifaktorielle Natur der Alzheimer-Krankheit wirksam zu adressieren.
Experteneinschätzung
Dr. Maria Alvarez, Neurowissenschaftlerin mit Schwerpunkt auf zellulärer Bioenergetik, kommentierte: „Diese Experimente liefern überzeugende kausale Hinweise darauf, dass ein Energiemangel in Neuronen Verhaltenssymptome antreiben kann. Der Ansatz mit mitoDREADD-Gs ist eine elegante Methode, die mitochondriale Aktivität zeitlich und räumlich präzise zu steuern. Für die Translation wird die Herausforderung darin bestehen, klinisch sichere Pharmakologien zu finden, die diese selektive Aktivierung nachahmen, ohne unerwünschte Nebenwirkungen zu verursachen.“
Dr. Alvarez fügt hinzu, dass zukünftige Studien eine Priorität auf longitudinale Arbeiten in gealterten Modellen legen und Kombinationen mit synapsenschützenden Therapien prüfen sollten, um zu beurteilen, ob mitochondriale Unterstützung neuronale Netzwerke über Monate oder Jahre erhalten kann statt nur Stunden oder Tage.
Nächste Schritte und zukünftige Perspektiven
Die Autorinnen und Autoren schlagen mehrere Folgerichtungen vor: Tests auf weitere Modelle der Neurodegeneration und psychiatrische Erkrankungen, die mit mitochondrialer Dysfunktion in Verbindung stehen; Kartierung der downstream-molekularen Pfade, die durch wiederhergestellte mitochondriale Aktivität ausgelöst werden; und Screening nach Wirkstoffkandidaten, die die Effekte von mitoDREADD-Gs in für Menschen kompatiblen Formulierungen reproduzieren können. Der translationale Weg erfordert ein robustes Sicherheitsprofil, die Optimierung von Liefermechanismen und Studien in großen Tiermodellen, bevor menschliche klinische Studien in Betracht gezogen werden können.
Wenn sich ein mitochondriales Versagen als kritisches frühes Ereignis in bestimmten Formen der Demenz erweist, könnte die Zielsetzung des zellulären Energiestoffwechsels ein wesentlicher Bestandteil einer mehrgleisigen therapeutischen Strategie werden. Selbst wenn die mitochondriale Dysfunktion nur ein Faktor unter vielen ist, könnten Interventionen, die die Energieversorgung der Neuronen verbessern, den Krankheitsverlauf verlangsamen oder die Wirksamkeit anderer Behandlungen erhöhen.
Die Forschung wurde in Nature Neuroscience veröffentlicht, und das experimentelle Werkzeug sowie die Daten liefern eine Roadmap für Teams, die die Rolle der Mitochondrien beim Altern des Gehirns und bei Erkrankungen untersuchen.
Fazit
Diese Studie liefert starke experimentelle Belege dafür, dass das direkte Anheben der mitochondrialen Aktivität in Neuronen Gedächtnis- und motorische Defizite in Mausmodellen der Demenz rückgängig machen kann und damit eine kausale Verbindung zwischen mitochondrialer Dysfunktion und neurodegenerativen Symptomen stützt. Während mitoDREADD-Gs selbst ein Laborwerkzeug und keine klinische Therapie ist, eröffnet es neue molekulare Ziele und experimentelle Ansätze, die die zukünftige Wirkstoffentwicklung informieren könnten. Kritische nächste Schritte sind die Bewertung langfristiger Effekte, Tests in verschiedenen Krankheitsmodellen und die Identifikation sicherer, für Menschen geeigneter Strategien zur Modulation der mitochondrialen Funktion als Teil umfassender Bemühungen, Alzheimer und verwandte Erkrankungen zu verhindern oder zu behandeln.
Quelle: sciencealert

Kommentar hinterlassen