6 Minuten
Ein möglicher universeller Ansatz für Krebsimpfungen
Forscher der University of Florida berichten über einen präklinischen Fortschritt, der die Reichweite therapeutischer Krebsimpfstoffe erweitern könnte. Anstatt das Immunsystem nur auf ein einzelnes tumorspezifisches Ziel zu trainieren, löst der neue mRNA-basierte Impfstoff einen allgemeinen, starken Immunalarm aus, der verschiedene Tumorzellen — einschließlich therapieresistenter Typen — für einen Immunangriff besser sichtbar macht. Die Studie, veröffentlicht in Nature Biomedical Engineering, zeigt in Mausmodellen anhaltende Tumorkontrolle und in einigen Fällen vollständige Rückbildung, wenn der Impfstoff mit Immun-Checkpoint-Inhibitoren kombiniert wird.
Wissenschaftlicher Hintergrund und Wirkmechanismus
Krebsimpfstoffe zielen darauf ab, das Immunsystem zu schulen, bösartige Zellen zu erkennen und zu zerstören. Konventionelle therapeutische Impfstoffe präsentieren in der Regel tumorspezifische Antigene, sodass T-Zellen ein definiertes Merkmal erkennen können. Allerdings entziehen sich viele Krebserkrankungen der Erkennung, indem sie diese Marker verändern oder eine immunsuppressive Mikroumgebung schaffen.
Die neue Strategie verwendet eine mRNA-Formulierung (von den Autoren als uRNA bezeichnet), die statt tumorspezifischer Antigene immunstimulierende Signalmoleküle codiert. Nach der Verabreichung weist die mRNA Zellen an der Injektionsstelle an, Zytokine und andere Immunmodulatoren zu produzieren, die angeborene und adaptive Immunwege aktivieren. Die Wirkung besteht darin, ruhende antigenpräsentierende Zellen zu „wecken“ und sie in eine anhaltende Anti-Tumor-Reaktion einzubinden.
Entscheidend ist, dass die aus der mRNA des Impfstoffs produzierten Moleküle nicht auf einen bestimmten Tumor zugeschnitten sind. Stattdessen verstärken sie Reaktionen sonst ruhender Immunzellen und verbessern die Erkennung eines breiteren Spektrums tumorassoziierter Merkmale. Bildlich gesprochen wirkt der Impfstoff wie eine universelle Sirene, die die „Grenzpolizei“ des Körpers alarmiert — die Überwachung wird über verschiedene Tumortypen und genetische Hintergründe hinweg erhöht.
Immune Checkpoint-Blockade als Partnertherapie
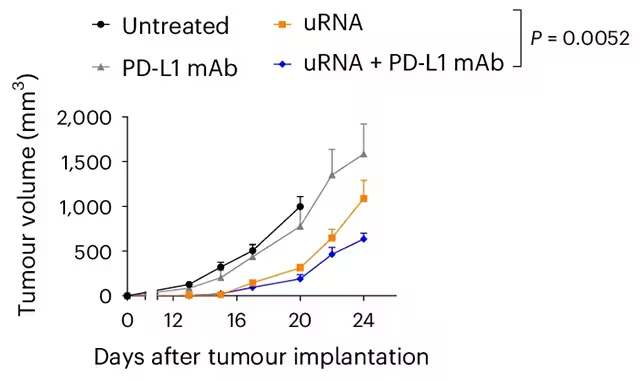
In der Studie kombinierten die Forschenden den mRNA-Impfstoff mit Immun-Checkpoint-Inhibitoren (ICIs) — konkret mit monoklonalen Antikörpern gegen PD-L1 (PD-L1 mAb). Checkpoint-Inhibitoren entfernen molekulare Bremsen, die die T-Zell-Aktivierung unterdrücken, und in Kombination mit einer impfinduzierten Steigerung der Immunvorbereitung können sie einen synergistischen Effekt erzeugen.
Viele Tumoren mit hoher Mutationslast oder adaptiven Resistenzmechanismen entgehen allein ICIs. In den Mausversuchen löste die Kombination aus uRNA und PD-L1 mAb eine starke Anti-Tumor-Immunität aus, kehrte die Resistenz in mehreren aggressiven Modellen um und beseitigte einige Tumoren vollständig. Die Autoren betonen, dass der Impfstoff zwar in einigen Fällen auch als Monotherapie aktiv war, die robustesten und reproduzierbarsten Reaktionen jedoch in Kombination mit der Checkpoint-Blockade auftraten.
Wesentliche Entdeckungen, Implikationen und nächste Schritte
Wesentliche Erkenntnisse aus der präklinischen Arbeit umfassen:
- Breite Immunsensibilisierung: Der mRNA-Impfstoff mobilisierte verschiedene Immunzelltypen und verbesserte die Erkennung von Tumorzellen, die von bestehenden Impfstoffen zuvor nicht adressiert wurden.
- Überwindung von Resistenz: Tumoren, die als resistent gegenüber Checkpoint-Blockade galten, wurden empfänglich, wenn der Impfstoff der ICI-Therapie vorausging oder sie begleitete.
- Vollständige Rückbildungen: Ein Teil der Mäuse erzielte eine vollständige Tumorabtötung, was in bestimmten Modellen potenzielle kurative Effekte anzeigt.
Die Implikationen sind bedeutsam für die Krebsimmuntherapie. Ein breit wirkender, „off-the-shelf“-Impfstoff könnte den Bedarf an patientenspezifischen Neoantigen-Impfstoffen verringern und den Zugang zur Immuntherapie für Patienten erweitern, deren Tumoren keine klar adressierbaren Antigene aufweisen. Wie der Onkologe Elias Sayour, der in der Studie zitiert wird, anmerkt: Dieser Ansatz liefert einen Proof-of-Concept für kommerzialisierbare universelle Krebsimpfstoffe, die das Immunsystem gegen individuelle Tumoren sensibilisieren.
Die Ergebnisse bleiben jedoch präklinisch. Wichtige nächste Schritte sind die Optimierung der Dosis, Sicherheitsprofilierung und sorgfältig geplante klinische Studien am Menschen, um Wirksamkeit und immunbedingte Nebenwirkungen zu bewerten. Das Team entwickelt neue mRNA-Formulierungen und plant Studien, um sowohl Therapie- als auch Rezidivpräventionsszenarien zu untersuchen.
Sicherheit, Auswahl und Einschränkungen
Die Modulation der Immunaktivierung birgt bekannte Risiken. Eine übermäßige oder fehlgeleitete Immunstimulation kann Autoimmunität, Zytokin-Freisetzungssyndrome oder organspezifische Toxizitäten verursachen. Die Bestimmung therapeutischer Fenster und prädiktiver Biomarker für die Patientenauswahl wird entscheidend sein, um diese Risiken zu mindern. Die Forschenden untersuchen außerdem, ob spezifische Immun- oder genetische Signaturen bessere Reaktionen auf das Impfstoff-plus-ICI-Regime vorhersagen.
Weitere Einschränkungen der aktuellen Arbeit ergeben sich aus den Beschränkungen von Mausmodellen, die die menschliche Tumorheterogenität, Mikroumgebungen oder langfristige Immunregulation nicht vollständig abbilden. Translationale Herausforderungen — Herstellung, Stabilität und Zulassungswege für ein universelles immunmodulatorisches mRNA-Produkt — müssen ebenfalls angegangen werden.
Expert Insight
Kommentar einer Wissenschaftskommunikatorin
„Diese Studie stellt eine wichtige konzeptionelle Verschiebung dar: Statt einen Impfstoff passgenau auf den Tumor zuzuschneiden, verstärkt sie die Fähigkeit des Immunsystems, den Tumor überhaupt wahrzunehmen“, sagt Dr. Amina Patel, Immunologin und Wissenschaftskommunikatorin. „Wenn sich dies beim Menschen sicher replizieren lässt, könnte eine solche Strategie die Anwendung von Immuntherapie bei vielen Krebsarten vereinfachen — aber das Sicherheitsprofil und eine sorgfältige Patientenauswahl werden ihren klinischen Wert bestimmen.“
Zukunftsaussichten und verwandte Technologien
Die Arbeit liegt am Schnittpunkt von mRNA-Therapeutika, Tumorimmunologie und der Entwicklung von Immunonkologika. Sie ergänzt andere Innovationen wie personalisierte Neoantigen-Impfstoffe, CAR-T-Zelltherapie und Kombinationsregime, die onkolytische Viren oder zielgerichtete Niedermoleküle einschließen. Fortschritte bei mRNA-Lieferplattformen, verbesserter Adjuvans-Design und prädiktiven Biomarkern für Immunantworten werden die Translation beschleunigen.
Forschende prüfen außerdem, ob ähnliche Impfstoffprinzipien Rezidive nach Operationen verhindern können und ob verschiedene Checkpoint-Ziele oder Dosierungsschemata die Ergebnisse weiter verbessern. Die Zusammenarbeit zwischen akademischen Gruppen, Biotech-Firmen und klinischen Konsortien wird entscheidend sein, um dieses Konzept in Humanstudien zu überführen.
Fazit
Die von der University of Florida geführte präklinische Studie beschreibt eine mRNA-Impfstoffstrategie, die die Anti-Tumor-Immunität breit aktiviert und in Kombination mit PD-L1-Checkpoint-Blockade therapieresistente Tumoren bei Mäusen eliminiert. Die Ergebnisse stützen das Konzept eines universellen Krebsimpfstoffs, der die Immunerkennung über verschiedene Tumore hinweg verbessert. Trotz vielversprechender Befunde erfordert der Ansatz sorgfältige klinische Prüfungen, um Sicherheit, optimale Kombinationen und die Patientengruppen zu bestimmen, die am meisten profitieren. Veröffentlicht in Nature Biomedical Engineering markiert die Studie einen wichtigen Schritt zur Erweiterung der Krebsimmuntherapie und unterstreicht das anhaltende Potenzial der mRNA-Technologie in der Onkologie.
Quelle: sciencealert

Kommentar hinterlassen