5 Minuten
Das Abschnüren der Blutversorgung von Geweben kann das Knochenmark vorzeitig altern lassen und das Immunsystem in einen krebs-toleranten Zustand verschieben, so eine neue Studie von NYU Langone Health, veröffentlicht in JACC: CardioOncology. In Mausmodellen für Brustkrebs verdoppelte vorübergehende Ischämie in einer Hintergliedmaße das Tumorwachstum im Vergleich zu Mäusen mit normaler Durchblutung. Die Experimente deuten darauf hin, dass periphere Ischämie — die verringerte Sauerstoffzufuhr durch verengte Arterien in den Beinen — Knochenmark-Stammzellen umprogrammiert und die Produktion von Immunzellen zugunsten populationsverschiebender, tumorunterdrückender Zelltypen verändert, statt sie anzugreifen. Bildnachweis: Shutterstock
Wissenschaftlicher Hintergrund: Ischämie, periphere arterielle Verschlusskrankheit und Krebsrisiko
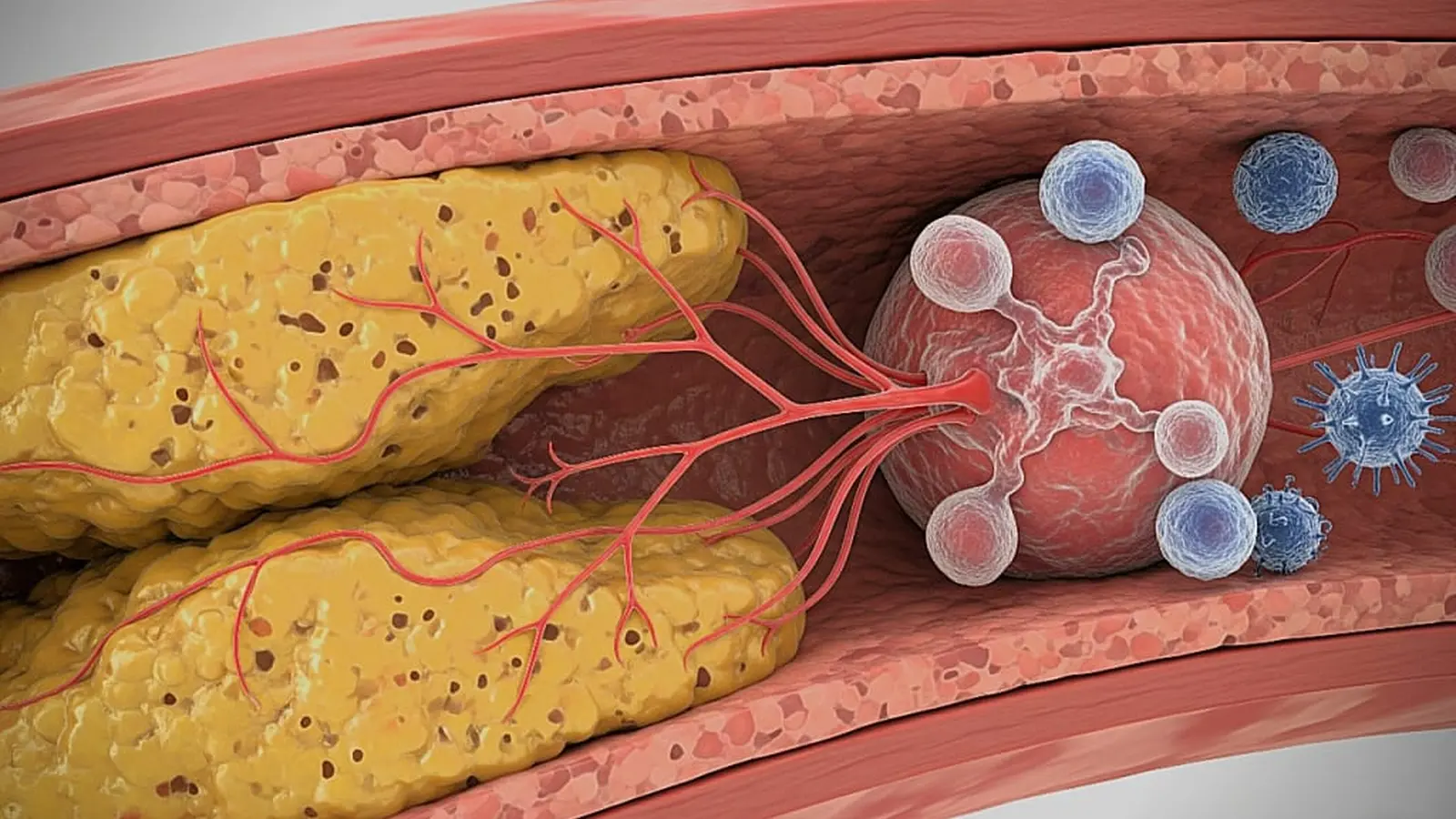
Ischämie entsteht, wenn Fett, Cholesterin und Entzündung Arterien verengen und die Zufuhr sauerstoffreicher Blutanteile einschränken. In den Beinen ist dieser Zustand als periphere arterielle Verschlusskrankheit (PAVK, engl. PAD) bekannt, die weltweit Millionen Menschen betrifft und das Risiko für Herzinfarkt und Schlaganfall erhöht. Die NYU-Forscher bauten auf früheren Arbeiten auf (einschließlich einer Studie aus 2020, die Ischämie nach Herzinfarkten mit schnellerem Tumorwachstum verband), um zu untersuchen, wie Ischämie außerhalb des Herzens die systemische Immunantwort und das Krebsprogressionsrisiko beeinflusst.
Das Immunsystem ist auf Knochenmark-Stammzellen angewiesen, um über die Lebenszeit weiße Blutkörperchen zu ersetzen und bereitzustellen. Bei normaler Durchblutung besteht ein Gleichgewicht zwischen entzündlichen Reaktionen (zum Beseitigen von Infektionen oder geschädigtem Gewebe) und regulatorischen Signalen, die Kollateralschäden begrenzen. Die NYU-Studie zeigt, dass Ischämie dieses Gleichgewicht stört, indem sie die Programmierung der Stammzellen im Mark verändert.
Methoden und zentrale Ergebnisse
Das Team verwendete ein kontrolliertes Mausmodell mit Brusttumoren und induzierte vorübergehende Ischämie in einer Hintergliedmaße, um PAVK zu simulieren. Sie verglichen Tumorprogression, Immunzellprofile und Genregulation zwischen ischämischen und Kontrolltieren.
Wesentliche Befunde:
- Das Tumorwachstum verdoppelte sich bei Mäusen mit Gliedmaßenischämie im Vergleich zu Kontrollen.
- Knochenmark-Stammzellen wurden umprogrammiert und bevorzugten die Bildung myeloider Linien (Monozyten, Makrophagen, Neutrophile), die mit Immunsuppression assoziiert sind.
- Die Produktion von Lymphozyten, insbesondere von T‑Zellen, die anti-tumorale Immunität vermitteln, nahm ab.
- Im Tumormikromilieu sammelten sich immunsuppressive Populationen, darunter Ly6Chi-Monozyten, M2‑ähnliche F4/80+ MHCIIlo‑Makrophagen und regulatorische T‑Zellen (Tregs).
- Ischämie führte zu dauerhaften Veränderungen in Hunderten von Genen und remodelte die Chromatinstruktur in Immunzellen, wodurch es schwieriger wurde, anti-krebs Programme zu aktivieren.
Mechanismus: Knochenmarkalterung und Immunsystem-Verschiebung
Die Autoren berichten, dass Ischämie effektiv ein vorzeitiges Alterungsphänotyp im Knochenmark induziert. Chromatin‑Umstrukturierungen und veränderte Genexpression verwandelten die Stammzellausbeute und erzeugten eine systemische Immunlandschaft, die Tumorwachstum toleriert. Wie die korrespondierende Autorin Kathryn J. Moore, PhD, feststellt: "Unsere Studie zeigt, dass beeinträchtigte Blutversorgung das Krebswachstum antreibt, unabhängig davon, wo im Körper sie auftritt. Dieser Zusammenhang zwischen peripherer arterieller Verschlusskrankheit und Brustkrebswachstum unterstreicht die entscheidende Bedeutung, metabolische und vaskuläre Risikofaktoren als Teil einer umfassenden Krebsbehandlungsstrategie anzugehen."
Dauerhafte Immun‑Reprogrammierung
Über eine vorübergehende Entzündungsreaktion hinaus erzeugte Ischämie langanhaltende epigenetische und transkriptionelle Verschiebungen. Diese stabilen Veränderungen erklären, warum ein lokales vaskuläres Ereignis die systemische Immunabwehr umgestalten und ein förderliches Umfeld für Krebsprogression schaffen kann.
Klinische Implikationen und zukünftige Richtungen
Diese Arbeit legt mehrere translationale Wege nahe: früheres Krebs-Screening für Patienten mit PAVK, klinische Studien, die testen, ob entzündungsmodulierende oder epigenetische Therapien ischämie‑getriebene Immunveränderungen rückgängig machen können, sowie integrierte Versorgungsstrategien, die sowohl vaskuläre Gesundheit als auch Krebsrisiko berücksichtigen. Die Erstautorin Alexandra Newman, PhD, bemerkt: "Diese Ergebnisse öffnen Türen für neue Strategien in Prävention und Behandlung von Krebs, etwa früheres Screening für Patientinnen und Patienten mit peripherer arterieller Verschlusskrankheit und den Einsatz entzündungshemmender Therapien, um diesen Effekten entgegenzuwirken."
Nächste Schritte
Das NYU-Team plant, klinische Studien zu unterstützen, die prüfen, ob zugelassene Antientzündungsmedikamente oder Wirkstoffe, die die Chromatinzugänglichkeit verändern, die antitumorale Immunität nach ischämischen Episoden wiederherstellen können.
Experteneinschätzung
Dr. Elena Sánchez, eine Forscherin in der Immuno‑Onkologie (fiktive Expertin zur Einordnung), kommentiert: "Die Studie verknüpft elegant vaskuläre Pathologie mit systemischer Immunalterung. Wenn ähnliche Mechanismen auch beim Menschen gelten, könnte das Screening auf Krebsrisiko bei PAVK‑Patienten eine wichtige präventive Maßnahme werden. Es weist zudem darauf hin, Entzündung und Gefäßerkrankungen zu behandeln, um die Immunüberwachung zu stärken."
Fazit
Die Studie von NYU Langone liefert mechanistische Hinweise darauf, dass gestörte Blutversorgung außerhalb des Tumors — etwa bei peripherer arterieller Verschlusskrankheit — Krebs beschleunigen kann, indem sie Knochenmark‑Stammzellen umprogrammiert und immunsuppressive Zellpopulationen fördert. Diese Ergebnisse verknüpfen vaskuläre Gesundheit mit Krebsprogression und heben den Wert integrierter kardiovaskulärer und onkologischer Versorgung, früherer Screenings für Risikogruppen sowie die Erforschung von Therapien hervor, die Entzündungen und epigenetische Veränderungen adressieren, um eine robuste anti-tumorale Immunantwort wiederherzustellen.
Quelle: sciencedaily

Kommentar hinterlassen