5 Minuten
Neuere Forschungen haben eine beunruhigende Hypothese gestärkt: Die Alzheimer-Krankheit könnte infektiöse Prozesse beinhalten, die außerhalb des Gehirns beginnen, unter anderem in der Mundhöhle. Mehrere Studien weisen inzwischen auf Porphyromonas gingivalis — das Bakterium, das am engsten mit chronischer Parodontitis (Zahnfleischerkrankung) assoziiert ist — als möglichen Mitverursacher der Alzheimer-Pathologie hin. Diese Vorstellung stellt die konventionelle Auffassung von Alzheimer als rein intrinsische neurodegenerative Erkrankung in Frage und eröffnet neue Ansätze für Diagnose und Therapie.
Wissenschaftlicher Hintergrund und weshalb P. gingivalis wichtig ist
Porphyromonas gingivalis ist ein gramnegatives, anaerobes Bakterium, das an chronischer parodontaler Entzündung beteiligt ist. Lang anhaltende Parodontitis begünstigt systemische Entzündungen und kann bakterielle Komponenten sowie Toxine in den Blutkreislauf freisetzen. In der Alzheimer-Forschung konzentrieren sich Untersuchungen auf zwei miteinander verknüpfte Phänomene: das Auftreten charakteristischer Proteine im Gehirn — Amyloid‑beta (Aβ) und hyperphosphoryliertes Tau — und das Vorkommen mikrobieller Antigene oder Enzyme, die diese Pathologie auslösen oder verschlimmern könnten.
Ein wichtiger Befund, veröffentlicht im Jahr 2019, identifizierte P. gingivalis‑DNA, bakterielle Proteine und toxische Proteasen, sogenannte Gingipains, in den Gehirnen verstorbener Menschen mit Alzheimer. Die Studie detektierte außerdem Gingipain‑Antigene in Gehirnen von Personen, die histologisch Alzheimer‑Pathologie zeigten, aber während ihres Lebens nicht an Demenz erkrankt waren. Dieses Muster legt nahe, dass eine bakterielle Invasion einem klinischen kognitiven Abbau vorausgehen könnte und nicht lediglich eine Folge schlechter Mundhygiene bei Demenzpatienten ist.
Studienangaben und zentrale Entdeckungen
In Laborversuchen, koordiniert von Cortexyme und geleitet von Forschern wie Jan Potempa und Stephen Dominy, kombinierten die Wissenschaftler Analysen menschlicher postmortaler Gehirne mit Tiermodellen. Zu den zentralen Beobachtungen gehörten:
- Nachweis von P. gingivalis‑genetischem Material und Gingipain‑Enzymen in Alzheimer‑Gehirnen, assoziiert mit Tau‑ und Ubiquitin‑Markern.
- Bei Mäusen führte eine orale Infektion mit P. gingivalis zu einer Besiedlung des Gehirns, erhöhter Aβ‑Produktion und neuroinflammatorischen Veränderungen, die einer Alzheimer‑ähnlichen Pathologie entsprachen.
- Ein von Cortexyme entwickelter Kleinmolekül‑Inhibitor, COR388 (Atuzaginstat), verringerte in Mausmodellen die bakterielle Belastung im Gehirn, reduzierte die Amyloid‑beta‑Produktion und dämpfte die Neuroinflammation in präklinischen Experimenten.
Diese Ergebnisse beweisen für sich genommen keine Kausalität beim Menschen, erfüllen jedoch mehrere Kriterien biologischer Plausibilität: ein plausibler Infektionsweg (Mundhöhle → systemischer Kreislauf → Gehirn), der Nachweis mikrobieller Komponenten im erkrankten Gewebe sowie die Modulation sowohl des mikrobiellen Vorhandenseins als auch krankheitsassoziierter Marker bei gezielter Hemmung der bakteriellen Proteasen.
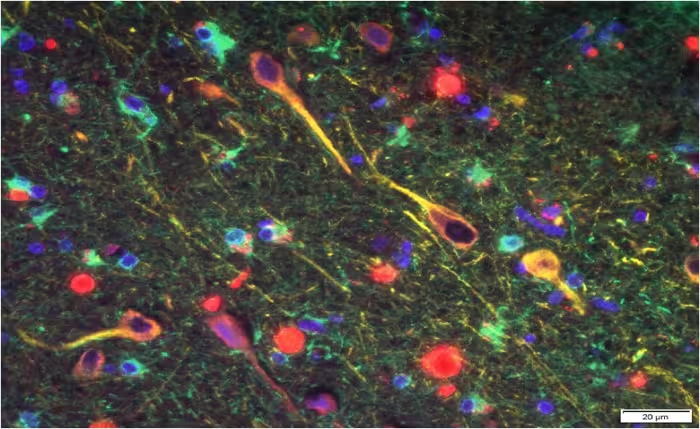
Marker und Mechanismen
Gingipains sind von P. gingivalis ausgeschiedene proteolytische Enzyme, die Wirtsproteine abbauen und Immunreaktionen modulieren können. Ihr Vorkommen korrelierte mit höheren Ausprägungen von Tau‑Pathologie und Ubiquitin‑Markierungen — Kennzeichen einer gestörten Proteinhomöostase in Neuronen. Auch Amyloid‑beta, lange Zeit mit Plaquebildung bei Alzheimer in Verbindung gebracht, war bei infizierten Mäusen erhöht, was die Hypothese stützt, dass Aβ als Teil einer angeborenen Immunantwort auf mikrobielle Invasion produziert werden könnte.
Folgen für Behandlung und Prävention
Wenn orale Krankheitserreger zur Progression von Alzheimer beitragen, könnten Strategien zur Reduktion von Parodontitis und zur gezielten Bekämpfung bakterieller Virulenzfaktoren Teil eines mehrgleisigen Ansatzes zur Prävention und frühen Intervention werden. Therapeutika, die darauf abzielen, Gingipains zu neutralisieren oder chronische orale Infektionen zu beseitigen, könnten bestehende Forschungsansätze zu Amyloid‑gerichteten Wirkstoffen und entzündungshemmenden Strategien ergänzen.
"Infektiöse Agenzien wurden zuvor mit der Entstehung und dem Fortschreiten der Alzheimer‑Krankheit in Verbindung gebracht, aber die Beweislage für Kausalität war nicht überzeugend", bemerkten Stephen Dominy und Mitarbeiter. "Jetzt haben wir erstmals solide Hinweise, die den intrazellulären, gramnegativen Erreger P. gingivalis mit der Alzheimer‑Pathogenese verbinden." David Reynolds von Alzheimer's Research fügte hinzu, dass, obwohl die bisherigen Nutzenergebnisse sich auf Tierstudien beschränken, die Erprobung vielfältiger Ansätze angesichts des langen Mangels an neuen Demenztherapien essenziell sei.
Experteneinschätzung
Dr. Elena Morales, Neurologin und Mikrobiomforscherin, kommentiert: „Dieses Forschungsfeld unterstreicht die Vernetzung von systemischer Gesundheit und Gehirngesundheit. Orale Erreger wie P. gingivalis können einen chronischen Entzündungszustand hervorrufen, der über Jahrzehnte hinweg ein vulnerables Gehirn in Richtung Neurodegeneration treiben kann. Das erklärt nicht alle Fälle von Alzheimer isoliert, legt aber nahe, dass praktische Präventionsschritte — verbesserte Parodontitis‑Versorgung und gezielte antimikrobielle Strategien — das Risiko senken könnten. Entscheidend sind große klinische Studien, um festzustellen, ob Interventionen, die orale Infektionen reduzieren, den Verlauf von Demenz beim Menschen verändern."
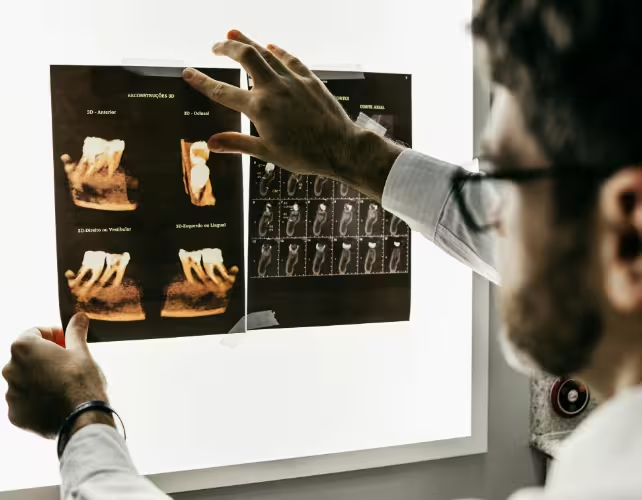
Verursacht Zahnfleischerkrankung Alzheimer, oder sind Menschen mit Demenz eher von schlechter Mundhygiene betroffen? (Jonathan Borba/Unsplash)
Fazit
Die Hinweise, orale Pathogene — insbesondere Porphyromonas gingivalis — mit Alzheimer‑typischen Hirnveränderungen zu verknüpfen, haben das Feld dahin gehend verschoben, Infektion und chronische Entzündung als beitragende Faktoren neurodegenerativer Prozesse zu betrachten. Zwar ist die Kausalität beim Menschen weiterhin nicht endgültig bewiesen, doch rechtfertigen der Nachweis von Gingipains und bakteriellen Signaturen in Alzheimer‑Gehirnen sowie unterstützende Tierdaten und frühe Wirkstoffkandidaten wie COR388 weitergehende klinische Untersuchungen. Bis dahin stellen gute Mundhygiene und Parodontalversorgung risikoarme Maßnahmen mit potenziellen langfristigen Vorteilen für die systemische und Gehirngesundheit dar.
Quelle: sciencealert

Kommentar hinterlassen