5 Minuten
Hintergrund: KRAS-Mutationen und dringender Handlungsbedarf bei Pankreas- und Darmkrebs
Pankreas- und Darmkrebs zählen zu den therapieresistentesten Tumorarten und treten nach operativen Eingriffen sowie Standardbehandlungen häufig erneut auf. Eine entscheidende Rolle spielt hierbei oft eine Mutation im KRAS-Onkogen, welches veränderte Signalproteine produziert und damit das Tumorwachstum begünstigt. In etwa 93% der Pankreaskarzinome und rund 50% der kolorektalen Karzinome lassen sich diese Mutationen nachweisen, weshalb KRAS als attraktives Ziel für neue Therapien gilt. Impfungen, die das Immunsystem darauf trainieren, Zellen mit mutiertem KRAS zu erkennen und zu vernichten, könnten Rückfälle verringern sowie die Überlebenszeit verlängern, sofern eine langanhaltende T-Zell-Antwort erreicht wird.
Studienaufbau und Wirkweise von ELI-002 2P
ELI-002 2P stellt eine sogenannte „off-the-shelf“-Peptidimpfung dar, die gezielt T-Zellen gegen gängige mutierte Formen des KRAS-Proteins aktiviert. Im Unterschied zu maßgeschneiderten, patientenspezifischen Impfstoffen, die individuell an die Tumormutationen einer Person angepasst werden, handelt es sich hierbei um ein standardisiertes Produkt, das großflächig einsetzbar ist. Die Vakzine verbindet KRAS-basierte Peptide mit einem Transportsystem, das den Impfstoff direkt in die Lymphknoten bringt, wo sich zahlreiche naive und Gedächtnis-Immunkellen befinden. Durch diese gezielte Präsentation des Antigens in lymphatischem Gewebe soll ein starker und spezifischer Ausbau von KRAS-mutierten T-Zellen gefördert werden.
Für die erste klinische Untersuchung wurden Patientinnen und Patienten aufgenommen, bei denen nach der operativen Entfernung des Primärtumors weiterhin ein hohes Rückfallrisiko bestand. Insgesamt nahmen 20 Menschen nach einem Pankreaseingriff und 5 Personen nach Entfernung eines Darmtumors teil. Das Studienschema umfasste wiederholte Impfungen sowie eine engmaschige immunologische Überwachung, um T-Zell-Antworten zu dokumentieren, ergänzt durch klinische Kontrollen zur Erfassung des rückfallfreien und des Gesamtüberlebens.
Zentrale Ergebnisse: Immunantworten und klinische Effekte
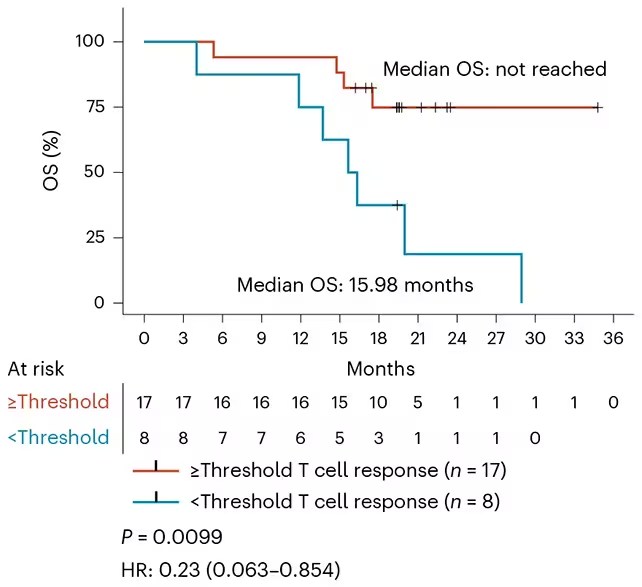
Die Auswertung fiel ausgesprochen vielversprechend aus. Bei der Mehrzahl der Teilnehmenden (84%) konnten spezifische T-Zellen gegen mutierte KRAS-Peptide nachgewiesen werden, was auf eine erfolgreiche Immunaktivierung hindeutet. Bei 24% der Patienten verschwanden nach der Impfung alle nachweisbaren Spuren von tumorgebundenen KRAS-Produkten im Blut oder Gewebe. Unter den 24 Personen mit den ausgeprägtesten Immunreaktionen waren zum letzten Follow-up-Termin 17 weiterhin krankheitsfrei, mit einer medianen Beobachtungszeit von fast 20 Monaten.
Im Gesamtkollektiv wurde ein medianes rückfallfreies Überleben von 16,33 Monaten und ein mittleres Gesamtüberleben von 28,94 Monaten erreicht – Werte, die im Vergleich zu den bisherigen Erwartungen für diese aggressiven Krebsarten als günstig gelten. Die Wissenschaftler beobachteten zudem Anzeichen dafür, dass durch ELI-002 2P hervorgerufene Immunantworten auch auf andere krebsassoziierte Veränderungen übergreifen können, was potenziell einen zusätzlichen klinischen Nutzen bei Tumoren mit hoher genetischer Vielfalt bietet.
Sicherheit und Verträglichkeit
Im Fokus der frühen Studienphase standen Sicherheit und Immunogenität. In dem kleinen Patientenkollektiv gab es keine überraschenden Sicherheitsbedenken, und das Vakzin wurde insgesamt gut vertragen. Dennoch sind größere Untersuchungen notwendig, um Nebenwirkungen und Langzeitrisiken umfassend einschätzen zu können.
Bedeutung, Expertenmeinung und Ausblick
Beteiligte Onkologen betonten die Tragweite dieser Ergebnisse für Tumore mit KRAS-Mutationen. Einer der Studienleiter merkte an, dass eine standardisierte Vakzine, die verlässlich KRAS-spezifische T-Zellen erzeugt, die Behandlung von Krebsarten grundlegend verändern könnte, die trotz Operation und Chemotherapie bislang häufig wiederkehren. Als standardisiertes Medikament kann ELI-002 2P zudem ohne die Zeitverzögerungen und hohen Kosten von Individualanfertigungen zur Verfügung gestellt werden, was die Anwendung für größere Patientengruppen erleichtert.
Zukünftige Forschungsanstrengungen sind notwendig: Randomisierte, kontrollierte Studien mit mehr Teilnehmenden sind entscheidend, um den Überlebensvorteil zu bestätigen, Patientenuntergruppen mit dem größten Nutzen zu definieren und Kombinationen mit anderen Immun- oder Zieltherapien zu testen. Zusätzliche Untersuchungen sollen Biomarker identifizieren, die das Ansprechen vorhersagen, sowie die Übertragbarkeit des Ansatzes auf andere onkogene Mutationen prüfen.
Fazit
Die ersten klinischen Erkenntnisse zu ELI-002 2P zeigen, dass eine auf Lymphknoten gerichtete, standardisierte Impfung in der Lage ist, wirksame T-Zell-Reaktionen gegen KRAS-mutierte Tumorzellen sicher hervorzurufen und klinische Resultate zu erreichen, die über den bisherigen Erwartungen für Pankreas- und Darmkrebspatienten liegen. Sollte sich dieser Ansatz in größeren Studien bewähren, könnte daraus eine skalierbare Immuntherapie zur Rückfallprävention und Lebensverlängerung bei KRAS-getriebenen Tumoren entstehen. Die Strategie unterstreicht darüber hinaus das Potenzial, durch mutationsgerichtete Tumorimpfstoffe eine gezielte und langanhaltende Tumorabwehr ohne die hohen Kosten und den Zeitbedarf vollständig personalisierter Verfahren bereitzustellen.
Quelle: nature

Kommentar hinterlassen